题目内容
15.向饱和澄清石灰水中加入少量CaC2,充分反应后恢复到原来的温度,所得溶液中( )| A. | c(Ca2+)、c(OH-)均增大 | |
| B. | 钙离子和氢氧根离子的物质的量均保持不变 | |
| C. | 钙离子和氢氧根离子的物质的量均减小 | |
| D. | c(OH-)增大、c(H+)减小 |
分析 加入CaC2,与水发生CaC2+2H2O=Ca(OH)2+HC≡CH↑,反应消耗水,结合Ca(OH)2(s)?Ca2+(aq)+2OH-(aq)的影响因素解答.
解答 解:加入CaC2,与水发生CaC2+2H2O=Ca(OH)2+HC≡CH↑,反应消耗水,因原溶液为饱和溶液,则反应后一定有Ca(OH)2析出,钙离子和氢氧根离子的物质的量均减小,温度不变,饱和澄清石灰水中中各离子浓度不变,
故选C.
点评 本题考查了难溶电解质的溶解平衡,侧重于学生的分析能力的考查,注意把握反应的原理以及溶解平衡的特点,难度不大.

练习册系列答案
相关题目
5.下列说法中正确的是( )
①${\;}_{17}^{35}$Cl、${\;}_{17}^{37}$Cl为不同的核素,有不同的化学性质
②元素周期表中元素排列顺序的依据是元素的相对原子质量
③原子的种类大于元素的种类
④所有的原子都含有质子、中子、电子
⑤质子数相同的微粒一定是同种元素
⑥质子数相同、电子数也相同的两种微粒,不可能一种是分子,另一种是离子
⑦同种元素的原子只能有一种质量数
⑧两原子如果核外电子排布相同,则一定属于同种元素
⑨第四、五、六周期称为长周期
⑩过渡元素包括了大部分金属元素.
①${\;}_{17}^{35}$Cl、${\;}_{17}^{37}$Cl为不同的核素,有不同的化学性质
②元素周期表中元素排列顺序的依据是元素的相对原子质量
③原子的种类大于元素的种类
④所有的原子都含有质子、中子、电子
⑤质子数相同的微粒一定是同种元素
⑥质子数相同、电子数也相同的两种微粒,不可能一种是分子,另一种是离子
⑦同种元素的原子只能有一种质量数
⑧两原子如果核外电子排布相同,则一定属于同种元素
⑨第四、五、六周期称为长周期
⑩过渡元素包括了大部分金属元素.
| A. | ①②③⑥⑧ | B. | ③⑥⑧⑨⑩ | C. | ②③⑤⑥⑦ | D. | ④⑤⑥⑨⑩ |
6.金秋十月,人们只要靠近盛开桂花的桂花树时,就能闻到怡人的桂花香.其原因是( )
| A. | 微粒体积很小 | B. | 微粒之间有间隔 | ||
| C. | 微粒质量很小 | D. | 微粒在不停的运动 |
20.关于如图所示装置的叙述,正确的是( )
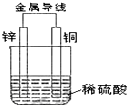

| A. | 铜是阳极,铜片上有气泡产生 | B. | 铜片质量不断减少 | ||
| C. | 电流从锌片经导线流向铜片 | D. | 氢离子在铜片表面被还原 |
7.乙烯产量是衡量一个国家石油化工发展水平的标志.下列关于乙烯说法正确的是( )
| A. | 与乙烷互为同分异构体 | B. | 分子中存在C≡C | ||
| C. | 能使酸性高锰酸钾溶液褪色 | D. | 分子中存在C=O |
4.某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2.下列对该溶液的叙述中,不正确的是( )
| A. | 该温度高于25℃ | |
| B. | 由水电离出来的H+的浓度是1.0×10-10 mol•L-1 | |
| C. | 加入NaHSO4晶体抑制了水的电离 | |
| D. | 该温度下加入等体积pH=12的NaOH溶液可使该溶液恰好呈中性 |
5. 我国在反兴奋剂问题上的坚决立场是支持“人文奥运”的重要体现.某种兴奋剂的结构如图,关于它的说法正确的是( )
我国在反兴奋剂问题上的坚决立场是支持“人文奥运”的重要体现.某种兴奋剂的结构如图,关于它的说法正确的是( )
 我国在反兴奋剂问题上的坚决立场是支持“人文奥运”的重要体现.某种兴奋剂的结构如图,关于它的说法正确的是( )
我国在反兴奋剂问题上的坚决立场是支持“人文奥运”的重要体现.某种兴奋剂的结构如图,关于它的说法正确的是( )| A. | 它的化学式为C20H25O3 | |
| B. | 该化合物只能发生取代反应 | |
| C. | 从结构上看,它属于醇类 | |
| D. | 从元素组成上看,它可以在氧气中燃烧生成CO2和水 |