题目内容
【题目】![]() 时,使用
时,使用![]() 调节溶液
调节溶液![]() 过程中,二元弱酸
过程中,二元弱酸![]() 溶液中含
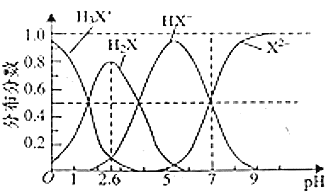
溶液中含![]() 微粒的分布分数如图所示。下列叙述中正确的是( )
微粒的分布分数如图所示。下列叙述中正确的是( )
A.溶液![]() 由1升至2.6时主要存在的反应是
由1升至2.6时主要存在的反应是![]()
B.![]() 溶液中
溶液中![]()
C.![]()
D.溶液呈中性时,![]()
【答案】C
【解析】
A.根据题图可知,当溶液![]() 由1升至2.6时,H3X+转化为H2X,其离子反应方程式为:H3X++OH-H2X+H2O,故A错误;
由1升至2.6时,H3X+转化为H2X,其离子反应方程式为:H3X++OH-H2X+H2O,故A错误;
B.有图像可知,当HX-含量较高时,溶液显酸性,即![]() 溶液显酸性,则溶液中c(H+)>c(OH-),故B错误;
溶液显酸性,则溶液中c(H+)>c(OH-),故B错误;
C.当溶液pH=7时,溶液中c(HX-)=c(X2-),即H2X的第二步电离平衡常数Ka2(H2X)=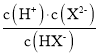 =10-7,故C正确;
=10-7,故C正确;
D.溶液呈中性时,根据电荷守恒有c(Na+)+ c(H+)= c(HX-)+2c(X2-)+ c(OH-),且c(H+)=c(OH-),则c(Na+)= c(HX-)+2c(X2-),故D错误;
答案选C。

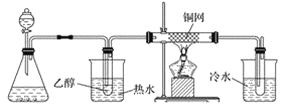
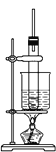
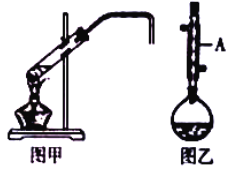
【题目】化学实验小组欲在实验室制备溴乙烷(图甲)和1﹣溴丁烷(图乙),涉及化学反应如下:
NaBr+H2SO4═HBr+NaHSO4 ①
C2H5﹣OH+HBrC2H5﹣Br+H2O ②
CH3CH2CH2CH2﹣OH+HBrCH3CH2CH2CH2﹣Br+H2O ③
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br﹣被浓硫酸氧化为Br2等。有关数据列表如下;
乙醇 | 溴乙烷 | 正丁醇 | 1﹣溴丁烷 | |
密度/gcm﹣3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
沸点/℃ | 78.5 | 38.4 | 117.2 | 111.6 |
请回答下列问题:
(1)图乙中仪器A的名称为_____。
(2)乙醇的沸点高于溴乙烷的沸点,其原因是_____。
(3)将1﹣溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在_____(填“上层”、“下层”或“不分层”)。
(4)制备操作中,加入的浓硫酸必需进行稀释,其目的是_____。(填字母)
A.减少副产物烯和醚的生成
B.减少Br2的生成
C.减少HBr的挥发
D.水是反应的催化剂
(5)欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是_____。(填字母)
A.NaIB.NaOHC.NaHSO3D.KCl
(6)制备溴乙烷(图甲)时,采用边反应边蒸出产物的方法,其有利于_____;但制备1﹣溴丁烷(图乙)时却不能边反应边蒸出产物,其原因是_____。
【题目】某研究性学习小组类比镁在二氧化碳中的燃烧反应,认为钠和二氧化碳也可以发生反应,他们对钠在CO2气体中燃烧进行了下列实验:
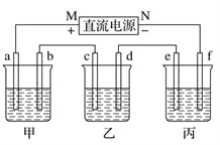
(1)若用下图装置制备CO2,则发生装置中反应的离子方程式为_________。
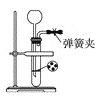
(2)将制得的CO2净化、干燥后由a口缓缓通入下图装置,待装置中的空气排净后点燃酒精灯,观察到玻璃直管中的钠燃烧,火焰为黄色。待冷却后,管壁附有黑色颗粒和白色物质。
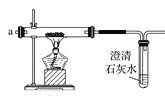
①能说明装置中空气已经排净的现象是_________。
②若未排尽空气就开始加热,则可能发生的化学反应方程式主要为_________。
(3)若钠着火,可以选用的灭火物质是_________。
A.水 B.泡沫灭火剂 C.干沙土 D.二氧化碳
(4)该小组同学对管壁的白色物质的成分进行讨论并提出假设:
Ⅰ.白色物质可能是Na2O; Ⅱ.白色物质可能是Na2CO3; Ⅲ.白色物质还可能是_________。
(5)为确定该白色物质的成分,该小组进行了如下实验:
实验步骤 | 实验现象 |
①取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加过量的CaCl2溶液 | 出现白色沉淀 |
②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
①通过对上述实验的分析,你认为上述三个假设中,___成立(填序号)。
②由实验得出:钠在CO2中燃烧的化学方程式为_____;每生成1mol氧化产物,转移的电子数为____。
(6)在实验(2)中还可能产生另一种尾气,该气体为________;处理该尾气的方法为_____。