题目内容
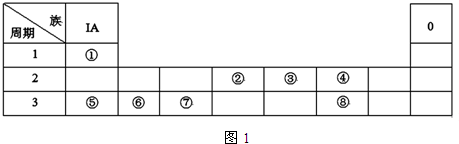
16.如表为元素周期表中短周期的一部分,关于A、B、C、D、E的说法正确的是( )| A | ||
| B | C | |
| D | E |
| A. | E的单质可与D的氢化物反应制得D的单质,所以非金属性:E>D | |
| B. | 对应的离子半径:E>D>C | |
| C. | 对应氢化物的熔沸点:B>D,因为B的氢化物分子内存在氢键 | |
| D. | B、C、D、E四种元素中,C的最高价氧化物对应的水化物酸性最强 |
分析 由短周期元素在周期表中的位置,可知A为He、B为O、C为F、D为S、E为Cl.
A.氯气能与硫化氢反应生成硫与HCl,说明氯的非金属性比硫的强;
B.电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大;
C.水分子之间存在氢键,熔沸点高于硫化氢;
D.F元素没有最高价含氧酸.
解答 解:由短周期元素在周期表中的位置,可知A为He、B为O、C为F、D为S、E为Cl.
A.氯气能与硫化氢发生反应:Cl2+H2S=S↓+2HCl,说明氯的非金属性比硫的强,故A正确;
B.电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径:S2>Cl->F-,故B错误;
C.水分子之间存在氢键,熔沸点高于硫化氢,故C正确;
D.F元素没有最高价含氧酸,故D错误,
故选AC.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,注意对元素周期表的掌握,难度不大.

练习册系列答案
相关题目
6.有A、B、C、D四块金属片,进行如下实验,①A、B用导线相连后,同时插入稀H2SO4中,A极为负极 ②C、D用导线相连后,同时浸入稀H2SO4中,电子由C→导线→D ③A、C相连后,同时浸入稀H2SO4,C极产生大量气泡 ④B、D相连后,同时浸入稀H2SO4中,D极发生氧化反应,则四种金属的活动性顺序为( )
| A. | A>B>C>D | B. | B>D>C>A | C. | C>A>B>D | D. | A>C>D>B |
11.已知Ⅰ、Ⅱ反应在一定条件下焓变及平衡常数如下:
2H2(g)+S2(g)?2H2S(g) K1;△H1 (Ⅰ)
3H2(g)+SO2(g)?2H2O(g)+H2S(g) K2;△H2 (Ⅱ)
(1)用△Hl、△H2表示反应4H2(g)+2SO2(g)?S2(g)+4H2O(g)的△H=△H2×2-△H1
(2)回答下列反应(I)的相关问题:
①温度为T1,在1L恒容容器中加入1.8molH2、1.2molS2,10min时反应达到平衡.测得10min内v(H2S)=0.08mol•L-1•min-1,则该条件下的平衡常数为0.8L•mol-1,若此时再向容器中充入H2(g)、S2(g)、H2S(g)各0.8mol,则平衡移动方向为正向(填“正向”、“逆向”或“不移动”);
②温度为T2时T2>T1,在1L恒容容器中也加入1.8molH2(g)、1.2molS2(g),反应建立平衡时测得S2(g)的转化率为25%,据此判断△H1<0(填“>”或“<”),与T1时相比,平衡常数K2减小(填“增大”、“减小”或“不变”).
(3)常温下,用SO2与NaOH溶液反应可得到NaHSO3、Na2SO3等.
①已知Na2SO3水溶液显碱性,原因是SO32-+H2O?HSO3-+OH-(写出主要反应的离子方程式),该溶液中,c(Na+)<2c(SO32-)+c(HSO3-)+c(OH-)(填“>”、“<”或“='’).
②在某NaHSO3、Na2SO3混合溶液中,HSO3-和SO32-物质的量之比与溶液pH变化如下表所示(部分):
根据表中数据,求盐Na2SO3溶液中SO32-的水解平衡常数K(SO32-)=10-6.2mol•L-1.
2H2(g)+S2(g)?2H2S(g) K1;△H1 (Ⅰ)
3H2(g)+SO2(g)?2H2O(g)+H2S(g) K2;△H2 (Ⅱ)
(1)用△Hl、△H2表示反应4H2(g)+2SO2(g)?S2(g)+4H2O(g)的△H=△H2×2-△H1
(2)回答下列反应(I)的相关问题:
①温度为T1,在1L恒容容器中加入1.8molH2、1.2molS2,10min时反应达到平衡.测得10min内v(H2S)=0.08mol•L-1•min-1,则该条件下的平衡常数为0.8L•mol-1,若此时再向容器中充入H2(g)、S2(g)、H2S(g)各0.8mol,则平衡移动方向为正向(填“正向”、“逆向”或“不移动”);
②温度为T2时T2>T1,在1L恒容容器中也加入1.8molH2(g)、1.2molS2(g),反应建立平衡时测得S2(g)的转化率为25%,据此判断△H1<0(填“>”或“<”),与T1时相比,平衡常数K2减小(填“增大”、“减小”或“不变”).
(3)常温下,用SO2与NaOH溶液反应可得到NaHSO3、Na2SO3等.
①已知Na2SO3水溶液显碱性,原因是SO32-+H2O?HSO3-+OH-(写出主要反应的离子方程式),该溶液中,c(Na+)<2c(SO32-)+c(HSO3-)+c(OH-)(填“>”、“<”或“='’).
②在某NaHSO3、Na2SO3混合溶液中,HSO3-和SO32-物质的量之比与溶液pH变化如下表所示(部分):
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
1.结晶牛胰岛素是中国科学家于1965年在世界上第一个人工合成的,其具有生物活性,那么结晶牛胰岛素本质上是什么( )
| A. | 糖类 | B. | 脂肪 | C. | 维生素 | D. | 蛋白质 |
8.Na2O2晶体中含有的化学键有( )
| A. | 离子键、σ键 | B. | 极性键、离子键 | C. | 离子键 | D. | 离子键、π键 |
5.下列化学反应中,属于氧化还原反应的是( )
| A. | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 | B. | NH3+HCl=NH4Cl | ||
| C. | 2Fe(OH)3$\frac{\underline{\;加热\;}}{\;}$Fe2O3+3H2O | D. | NaOH+HNO3=NaNO3+H2O |
6.二甲苯的苯环上有一个氢原子被溴取代后的一溴代物有六种异构体,它们的熔点分别如下表所示.下列叙述正确的是( )
| 二甲苯一溴代物的熔点(℃) | 234 | 206 | 214 | 204 | 212 | 205 |
| 对应的二甲苯的熔点(℃) | 13 | -48 | -25 | -48 | -25 | -48 |
| A. | 点为234℃的是一溴代间二甲苯 | B. | 熔点为234℃的是一溴代邻二甲苯 | ||
| C. | 熔点为-48℃的是间二甲苯 | D. | 熔点为-25℃的是对二甲苯 |