题目内容
【题目】CH4﹣O2燃料电池具有放电稳定,无污染等优点,如图为一用甲烷氧气燃料电池电解饱和氯化钠溶液的模型图。请认真读图,回答以下问题:
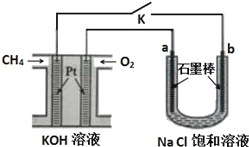
(1)请写出通入甲烷气体的一极所发生的电极反应式:____________________,其附近的pH值___(填“不变”或“变大”或“变小”)
(2)如果通入1mol的甲烷完全参与电极反应,则电路中转移_____________的电子,a电极产生的气体在标准状况下的体积为_________________。
【答案】 CH4﹣8e﹣+10OH﹣═CO32﹣+7H2O 变小 8mol 89.6L
【解析】试题分析:本题考查甲烷燃料电池的工作原理和电极反应式的书写,多池串联的计算。
(1)通入甲烷的一极为负极,由于电解质溶液为KOH溶液,CH4在负极被氧化成CO32-,电极反应式为CH4-8e-+10OH-=CO32-+7H2O。由于消耗OH-,c(OH-)减小,其附近的pH变小。
(2)根据电极反应式,1mol甲烷参与反应,电路中转移8mol电子。a极与甲烷燃料电池的正极相连,a极为阳极,a极电极反应为2Cl--2e-=Cl2↑,电路中转移8mol电子,a极生成的Cl2物质的量为4mol,在标准状况下的体积为4mol![]() 22.4L/mol=89.6L。
22.4L/mol=89.6L。

练习册系列答案
相关题目