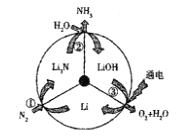
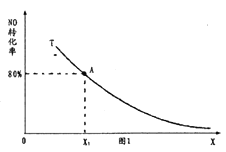
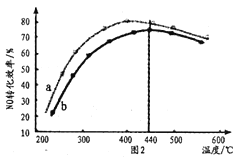
ΧβΡΩΡΎ»ί
ΓΨΧβΡΩΓΩΡ≥ΙΛ≥ß“‘œθΥαΈΣ‘≠Νœ…ζ≤ζ―«œθΥαΡΤΘ§ΤδΙΛ“’Νς≥Χ»γΆΦΘΚ
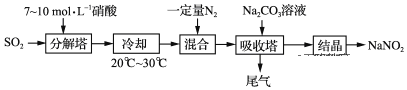
“―÷ΣΘΚNa2CO3+NO+NO2=2NaNO2+CO2
Θ®1Θ©ΓΑΖ÷ΫβΥΰΓ±÷–SO2¥”ΥΰΒΉΫχ»κΘ§œθΥα¥”ΥΰΕΞ≈γΝήΘ§ΤδΡΩΒΡ «____ΓΘ
Θ®2Θ©ΓΑΖ÷ΫβΥΰΓ±÷–ΒΡΈ¬Ε»≤Μ“ΥΙΐΗΏΘ§Τδ‘≠“ρ «____ΓΘ
Θ®3Θ©Α¥“ΜΕ®ΦΤΝΩ±»‘ΎΓΑΖ÷ΫβΥΰΓ±÷–Ά®SO2ΚΆ≈γ»κœθΥαΘ§»τΖ¥”ΠΚσ…ζ≥…ΒΡNO”κNO2Έο÷ ΒΡΝΩ÷°±»«ΓΚΟ1ΘΚ1Θ§‘ρΓΑΖ÷ΫβΥΰΓ±÷–ΖΔ…ζΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣ____ΓΘ
Θ®4Θ©ΈΣΧαΗΏΒΣ―θΜ·ΈοΒΡΉΣΜ·¬ Θ§Ω…œρΓΑΈ≤ΤχΓ±÷–Ά®»κ“ΜΕ®ΝΩΒΡ____ΤχΧεΘ§‘ΌΆ®»κΓΑΈϋ ’ΥΰΓ±÷–Θ§ Βœ÷―≠ΜΖΈϋ ’ΓΘ
Θ®5Θ©ΓΑΈϋ ’ΥΰΓ±ΥυΒΟ»ή“Κ÷–≥ΐΚ§”–NaNO2ΓΔNaNO3ΚΆ…ΌΝΩNa2CO3ΆβΘ§ΜΙΚ§”–ΒΡ»ή÷ ΈΣ___Θ®ΧνΜ·―ß ΫΘ©ΓΘ
ΓΨ¥πΑΗΓΩ ΙSO2ΤχΧε±Μ≥δΖ÷Έϋ ’ œθΥα ή»»ΜαΜ”ΖΔΓΔΖ÷Ϋβ 2HNO3+2SO2+H2O=NO+NO2+2H2SO4 O2 NaHCO3
ΓΨΫβΈωΓΩ
(1) ΓΑΖ÷ΫβΥΰΓ±÷–SO2¥”ΥΰΒΉΫχ»κΘ§œθΥα¥”ΥΰΕΞ≈γΝήΘ§ΤδΡΩΒΡ « ΙSO2ΤχΧε±Μ≥δΖ÷Έϋ ’ΘΜ
(2) ΓΑΖ÷ΫβΥΰΓ±÷–ΒΡΈ¬Ε»≤Μ“ΥΙΐΗΏΘ§Τδ‘≠“ρ «Έ¬Ε»ΧΪΗΏΘ§œθΥαΜαΜ”ΖΔΓΔΖ÷ΫβΘΜ
(3)Α¥“ΜΕ®ΦΤΝΩ±»‘ΎΓΑΖ÷ΫβΥΰΓ±÷–Ά®SO2ΚΆ≈γ»κœθΥαΘ§SO2 ±Μ―θΜ·Θ§‘ΎΥα–‘ΧθΦΰœ¬…ζ≥…H2SO4, HNO3±ΜΜΙ‘≠Θ§»τΖ¥”ΠΚσ…ζ≥…ΒΡNO”κNO2Έο÷ ΒΡΝΩ÷°±»«ΓΚΟ1 : 1Θ§ΗυΨίΒΟ ßΒγΉ” ΊΚψΘ§‘ρΓΑΖ÷ΫβΥΰΓ±÷–ΖΔ…ζΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣ2HNO3+2SO2+H2O= NO+NO2 t 2H2SO4ΘΜ
(4)”…”ΎNO≤Μ»ή”ΎNa2CO3Θ§ΈΣΧαΗΏΒΣ―θΜ·ΈοΒΡΉΣΜ·¬ Θ§Ω…œρΓΑΈ≤ΤχΓ±÷–Ά®»κ“ΜΕ®ΝΩΒΡO2ΤχΧεΘ§ ΙNO≤ΩΖ÷ΉΣΜ·ΈΣNO2Θ§‘ΌΆ®»κΓΑΈϋ ’ΥΰΓ±÷–Θ§ Βœ÷―≠ΜΖΈϋ ’ΘΜ
(5)Ϋχ»κΓΑΈϋ ’ΥΰΓ±ΒΡΜλΚœΤχΧε÷– «NOΓΔNO2Θ§Ζ¥”ΠΚσ”÷…ζ≥…ΝΥCO2Θ§ CO2±ΜNa2CO3Έϋ ’…ζ≥…ΝΥNaHCO3Θ§Ι ΓΑΈϋ ’ΥΰΓ±ΥυΒΟ»ή“Κ÷–≥ΐΚ§”–NaNO2ΓΔNaNO3ΚΆ…ΌΝΩNa2CO3ΆβΘ§ΜΙΚ§”–ΒΡ»ή÷ ΈΣNaHCO3ΓΘ

ΓΨΧβΡΩΓΩΡΤΦΑΤδΜ·ΚœΈοΨΏ”–ΙψΖΚΒΡ”ΟΆΨΓΘ
(1)≥ΘΈ¬œ¬Θ§≈®Ε»ΨυΈΣ0.1 mol/LΒΡœ¬Ν–Έε÷÷ΡΤ―Έ»ή“ΚΒΡpH»γ±μΥυ ΨΘΚ
»ή÷ | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
…œ ωΦΗ÷÷ΡΤ―ΈΒΡ“θάκΉ”Θ§ΫαΚœ«βάκΉ”ΡήΝΠΉν«ΩΒΡ «______(ΧνάκΉ”ΖϊΚ≈)Θ§ΗυΨί±μ÷– ΐΨίΘ§ΫΪ≈®Ε»ΨυΈΣ0.01mol/LΒΡœ¬Ν–ΥΡ÷÷»ή“ΚΖ÷±πœΓ Ά100±ΕΘ§pH±δΜ·Ήν¥σΒΡ «______.(ΧνΉ÷ΡΗ)ΓΘ
A.HCN B.HClO C.CH3COOH D.H2CO3
(2)“―÷ΣΦΗ÷÷άκΉ”ΩΣ Φ≥ΝΒμ ±»ή“ΚΒΡpH»γœ¬±μΥυ ΨΘΚ
άκΉ” | Fe2ΘΪ | Cu2ΘΪ | Mg2ΘΪ |
pH | 7.6 | 5.2 | 10.4 |
Β±œρΚ§”–œύΆ§≈®Ε»ΒΡCu2ΘΪΓΔMg2ΘΪΓΔFe2ΘΪΒΡ»ή“Κ÷–ΒΈΦ”«β―θΜ·ΡΤ»ή“Κ ±Θ§________(ΧνάκΉ”ΖϊΚ≈)œ»≥ΝΒμΘΜKsp[Fe(OH)2]______(ΧνΓΑΘΨΓ±ΓΑΘΫΓ±ΜρΓΑΘΦΓ±)Ksp[Mg(OH)2]ΘΜ“Σ Ι0.2 mol/LΒΡΝρΥαΆ≠»ή“Κ÷–Ά≠άκΉ”≥ΝΒμΫœΈΣΆξ»Ϊ( ΙΆ≠άκΉ”ΒΡ≈®Ε»ΫΒ÷Ν‘≠ά¥ΒΡ«ßΖ÷÷°“Μ)Θ§‘ρ”Πœρ»ή“Κ÷–Φ”»κ«β―θΜ·ΡΤ»ή“Κ Ι»ή“ΚpH=_______ΓΘ{Cu(OH)2ΒΡKsp=2ΓΝ10-20ΓΘ}