题目内容
一定温度下,在2 L的密闭容器中发生如下反应:A(s)+2B(g)  2C(g) ΔH<0,反应过程中B、C的物质的量随时间变化的关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图2.下列有关说法正确的是
2C(g) ΔH<0,反应过程中B、C的物质的量随时间变化的关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图2.下列有关说法正确的是
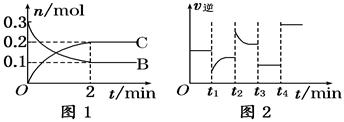
A.反应开始2 min内,v(B)=0.1 mol/(L·min)
B.t1时改变的条件可能是升高温度
C.t3时改变的条件可能是加压,此时c(B)不变
D.t4时可能是使用了催化剂,此时c(B)不变
 2C(g) ΔH<0,反应过程中B、C的物质的量随时间变化的关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图2.下列有关说法正确的是
2C(g) ΔH<0,反应过程中B、C的物质的量随时间变化的关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图2.下列有关说法正确的是
A.反应开始2 min内,v(B)=0.1 mol/(L·min)
B.t1时改变的条件可能是升高温度
C.t3时改变的条件可能是加压,此时c(B)不变
D.t4时可能是使用了催化剂,此时c(B)不变
D
反应开始2 min内,B的物质的量减少了0.2mol,所以v(B)=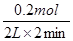 =0.05 mol/(L·min),A不正确;升高温度反应速率应该是增大的,B不正确;反应前后体积不变,增大压强平衡不移动,但物质的浓度是增大的,C不正确;催化剂只能改变反应速率,但不能影响平衡状态,所以D正确,答案选D。
=0.05 mol/(L·min),A不正确;升高温度反应速率应该是增大的,B不正确;反应前后体积不变,增大压强平衡不移动,但物质的浓度是增大的,C不正确;催化剂只能改变反应速率,但不能影响平衡状态,所以D正确,答案选D。
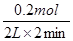 =0.05 mol/(L·min),A不正确;升高温度反应速率应该是增大的,B不正确;反应前后体积不变,增大压强平衡不移动,但物质的浓度是增大的,C不正确;催化剂只能改变反应速率,但不能影响平衡状态,所以D正确,答案选D。
=0.05 mol/(L·min),A不正确;升高温度反应速率应该是增大的,B不正确;反应前后体积不变,增大压强平衡不移动,但物质的浓度是增大的,C不正确;催化剂只能改变反应速率,但不能影响平衡状态,所以D正确,答案选D。
练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案
相关题目
 N2O4(g) ΔH <0,达到平衡后,下列说法不正确的是
N2O4(g) ΔH <0,达到平衡后,下列说法不正确的是 2NH3,△H<0的关系的是( )
2NH3,△H<0的关系的是( )
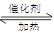 7N2+12 H2O可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。
7N2+12 H2O可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。 2SO3(g) ΔH= —196.6 kJ·mol-1
2SO3(g) ΔH= —196.6 kJ·mol-1 cC(g)。该反应达到平衡后,测得A气体的浓度为0.5mol/L。在恒温下将密闭容器扩大到原来的2倍,再次达到平衡后,测的A的浓度为0.3mol/L,则下列叙述正确的是
cC(g)。该反应达到平衡后,测得A气体的浓度为0.5mol/L。在恒温下将密闭容器扩大到原来的2倍,再次达到平衡后,测的A的浓度为0.3mol/L,则下列叙述正确的是 xC(g)+yD(g),达到平衡时C的体积分数为m%,若维持温度、压强不变,将0.6 L A、0.4 L B、4 L C、0.8 L D作为起始物质充入密闭容器内,达到平衡时C的体积分数仍为m%,则x=________,y=________.
xC(g)+yD(g),达到平衡时C的体积分数为m%,若维持温度、压强不变,将0.6 L A、0.4 L B、4 L C、0.8 L D作为起始物质充入密闭容器内,达到平衡时C的体积分数仍为m%,则x=________,y=________. 2SO3在一定温度下达到平衡,下列说法正确的是( )
2SO3在一定温度下达到平衡,下列说法正确的是( )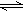 2C(g)+D(g)。当x在一定范围内变化时,均可以通过调节反应器的温度,使反应达到平衡时保持容器中气体总物质的量为5mol。若使起始反应向正反应方向进行,则x的取值范围下列适合的是( )
2C(g)+D(g)。当x在一定范围内变化时,均可以通过调节反应器的温度,使反应达到平衡时保持容器中气体总物质的量为5mol。若使起始反应向正反应方向进行,则x的取值范围下列适合的是( )