题目内容
【题目】如图为番茄电池,下列说法正确的是( )
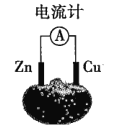
A.锌电极是该电池的正极B.铜电极附近会出现蓝色
C.一段时间后,锌片质量会变小D.电子由铜通过导线流向锌
【答案】C
【解析】
根据金属的活泼性知,锌作负极,铜作正极,负极上锌失电子发生氧化反应,正极上得电子发生还原反应,电子从负极沿导线流向正极,电流从正极沿导线流向负极。
A.该原电池中,锌作负极,负极上锌失电子生成锌离子进入溶液,所以锌片的质量会变小,故A错误;
B.铜作正极,正极上氢离子得电子生成氢气,所以铜电极附近不会出现蓝色,故B错误;
C.锌作负极,锌失去电子,导致锌片质量会变小,故C正确;
D.锌作负极,铜作正极,电流从铜沿导线流向锌,电子流向与电流相反,故D错误;
故答案选C。

 名校课堂系列答案
名校课堂系列答案【题目】利用如图所示装置进行以下实验,能得到相应实验结论的是( )
选项 | ① | ② | ③ | 实验结论 |
|
A | 浓氨水 | NaOH | 酚酞 | NaOH 的碱性比 NH3·H2O 的强 | |
B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
C | 浓硫酸 | Cu | Na2S | SO2 具有氧化性 | |
D | 浓硝酸 | Na2CO3 | Na2SiO3 | 非金属性:N>C>Si |
A.AB.BC.CD.D
【题目】用如图所示装置(夹持已装置省略)进行下列实验,能得出相应实验结论的是
选项 | ① | ② | ③ | 实验结论 |
|
A | 稀硫酸 | Na2S | AgNO3与AgCl的浊液 | Ksp(AgCl)>Ksp(Ag2S) | |
B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
C | 稀硫酸 | Na2CO3 | CaCl2溶液 | CO2可与氯化钙反应 | |
D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
A. AB. BC. CD. D
【题目】已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O.
某化学小组根据上述反应原理进行下列实验:
I.测定H2C2O4溶液的物质的量浓度
实验步骤如下:
①取待测H2C2O4溶液25.00mL放入锥形瓶中,再加入适量的稀硫酸;
②用0.1mol/LKMnO4溶液滴定至终点,记录数据;
③重复滴定2次,平均消耗KMnO4溶液20.00mL。
请回答:
(1)滴定时,将KMnO4溶液装在______(填“酸式”或“碱式”)滴定管中。
(2)若在步骤①操作之前,先用待测H2C2O4溶液润洗锥形瓶,则测得H2C2O4溶液的浓度会______(填“偏大”“偏小”或“无影响”)。
(3)步骤②中到达滴定终点时的现象为_______________________________。
(4)计算H2C2O4溶液的物质的量浓度为__________mol/L。
II.探究反应物浓度对化学反应速率的影响设计如下实验方案(实验温度均为25℃):
实验序号 | 体积V/mL | |||
0.1molL-1KMnO4溶液 | 0.11molL-1H2C2O4溶液 | 0.11molL-1H2SO4溶液 | H2O | |
① | 2.0 | 5.0 | 6.0 | 7.0 |
② | 2.0 | 8.0 | 6.0 | V1 |
③ | 2.0 | V2 | 6.0 | 2.0 |
请回答:
(5)表中v1=______。
(6)实验中需要测量的数据是______________________________。
(7)实验中______(填“能”或“不能”)用0.2mol/L盐酸代替0.1mol/LH2SO4溶液,理由是_________。