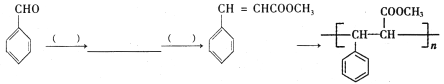
题目内容
【题目】短周期元素A、B、C、D,它们的原子序数依次增大。其中A、C与B、D分别是同主族元素。又知B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数和的2倍。这四种元素的单质中有2种气体,2种固体。
(1)写出元素符号:A______;B______;
(2)写出元素D在元素周期表中的位置______;
(3)写出C元素的单质与B元素的单质在常温下反应的化学方程式______;
(4)写出两种均含有A、B、C、D四种元素的化合物相互作用逸出气体的离子方程式______;
(5)A、C组成的化合物,常作为野外考察的取氢(H2)剂。该化合物中加入适量的水,即可形成氢气。写出制氢化学方程式______。
【答案】 H O 第三周期VIA族 4Na+O2![]() 2Na2O HSO3+H+
2Na2O HSO3+H+![]() SO2+H2O NaH+H2O
SO2+H2O NaH+H2O![]() NaOH+H2
NaOH+H2
【解析】A、B、C、D是4种短周期的元素,它们的原子序数依次增大,A、C及B、D分别是同一主族元素,B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数之和的2倍,这说明A应该是第一周期元素,则A为H元素,结合原子序数可知C为Na;B、D分别位于二、三周期,B、D的质子数之和为24,则B为O元素、D为S元素。
(1)由上述分析可知,A为H元素、B为O元素;(2)S元素位于元素周期表的第三周期VIA族;(3)C元素的单质与B元素的单质在常温下反应生成氧化钠,反应的化学方程式为4Na+O2=2Na2O;(4)均由A、B、C、D四种元素的两种化合物能发生反应且逸出气体,应是NaHSO3、NaHSO4,该反应的离子方程式为HSO3+H+=SO2↑+H2O;(5)A、C组成的化合物,常作为野外考察的取氢(H2)剂,该化合物中加入适量的水,即可形成氢气,化合物是NaH,制氢的化学方程式为NaH+H2O=NaOH+H2↑。

【题目】为研究哈伯法合成氨反应,T℃时,在容积为2 L恒容容器中通入4 mol N2和12mol H2,反应如下: N2(g)+3H2(g) ![]() 2NH3(g) △H=-92.0kJmol-1,相关键能数据如下:
2NH3(g) △H=-92.0kJmol-1,相关键能数据如下:
N≡N | H-H | N-H | |
键能数据( kJ/mol) | 946 | 436 | X |
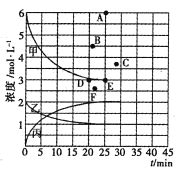
若25min时反应达到平衡,各物质浓度随时间变化曲线如下图中甲、乙、丙。回答下列问题:
(1)0-25min内,反应的平均速率v(H2)为_________;表中X=_________________。
(2)T℃时,该反应的平衡常数K=_____________ (用最简分数表达)。
(3)T℃时,若起始充入8mol N2和24 mol H2,则反应刚达到平衡时,表示c( H2)在右图中相应的点为_____(填字母)。
(4)以煤为主要原料的合成氨工业中,原料气氢气常用下述方法获得:
①C(s) +H2O(g)![]() CO(g) +H2(g) △H1
CO(g) +H2(g) △H1
②CO(g) +H2O(g)![]() CO2(g) +H2(g) △H2
CO2(g) +H2(g) △H2
若已知CO和H2的燃烧热分别为283 kJ·mol-l和285.8kJ·mol-l;H2O( g) =H2O(1) △H =-44kJ·mol-l 则△H2=_______________。
(5)氨气是生产硝酸的重要原料,其过程如下:
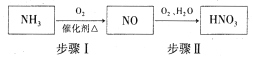
写出步骤I的化学方程式:_________________。
(6)下图是科学家提出的利用电解法常温常压下由氮气、氢气合成氨的示意图:
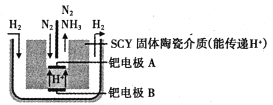
由图可知,钯电极B是电解池的________(填“阴极”或“阳极”);钯电极A上的电极反应式为________。