题目内容
【题目】 氨是氮循环过程中的重要物质,氨的合成是目前普遍使用的人工固氮方法。
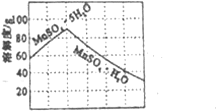
(1)根据下图提供的信息,写出该反应的热化学方程式
_____________________________________________,
下图的曲线中____________(填“a” 或“b”)表示 加入铁触媒(催化剂)的能量变化曲线。

(2)在恒容容器中,下列描述中能说明上述反应已达平衡的是_________________。
A.3υ(H2)正=2υ(NH3)逆
B.单位时间内生成n mol N2的同时生成2n molNH3
C.容器内气体的密度不随时间的变化而变化
D.容器内压强不随时间的变化而变化
(3)为了寻找合成NH3的适宜条件,某同学设计了三组实验(如下表),请在下表空格处填入相应的实验条件及数据。
实验编号 | T(℃) | n (N2)/n(H2) | P(MPa) |
ⅰ | 450 | 1/3 | 1 |
ⅱ | ______ | 1/3 | 10 |
ⅲ | 480 | ______ | 10 |
(4)合成氨的原料气氢气制备时其中一步反应: H2O(g)+CO(g)![]() CO2(g)+H2(g),在850 ℃时,其平衡常数K=1。若850 ℃时向体积为1 L的恒容密闭容器中,同时充入1.0 mol CO,3.0 mol H2O,1.0 mol CO2,5.0 mol H2,此时反应向____________(填“正反应”或“逆反应”)方向进行,平衡时CO2的物质的量为______________。
CO2(g)+H2(g),在850 ℃时,其平衡常数K=1。若850 ℃时向体积为1 L的恒容密闭容器中,同时充入1.0 mol CO,3.0 mol H2O,1.0 mol CO2,5.0 mol H2,此时反应向____________(填“正反应”或“逆反应”)方向进行,平衡时CO2的物质的量为______________。
【答案】 N2(g) + 3H2(g)![]() 2NH3(g) ΔH=-92 kJ·mol-1 b B D 450 1/3 逆反应 0.8 mol
2NH3(g) ΔH=-92 kJ·mol-1 b B D 450 1/3 逆反应 0.8 mol
【解析】(1)由图1可知,1molN2(g)与3molH2(g)完全反应生成2molNH3(g)的反应热为508kJ/mol-600kJ/mol=-92kJ/mol,所以合成氨的热化学反应方程式为N2(g)+3H2(g)2NH3(g)△H═-92kJ/mol,催化剂能降低反应的活化能,b活化能较低;
(2)A.3υ(H2)正=2υ(NH3)逆说明:v (NH3)逆:v (H2)正═3:2不等于对应化学计量数之比,即正反应速率不等于逆反应速率,故A错误; B.单位时间内生成nmolN2的同时生成2nmolNH3说明正反应速率等于逆反应速率,故B正确;C.体积不变,气体的质量不变,密度也会不变,用密度不变无法区分非平衡状态和平衡状态,故C错误;D.反应N2(g)+3H2(g)2NH3(g)是反应前后气体的总物质的量不相等的反应,当体积固定时,根据阿伏伽德罗定律可知,温度、体积相同时,气体的物质的量之比等于压强之比,容器内气压不随时间变化,说明气体的总物质的量不再发生变化,即说明可逆反应达到了化学平衡状态,故D正确;故选BD;
(3)该实验为了寻找合成NH3的适宜条件,ⅱ应只改变压强,ⅲ应只改变温度,所以应填入的数据为:450; ![]() ;
;
(4)Qc=![]() =
=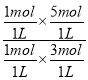 =
=![]() >1,故此时平衡向逆反应移动,设平衡时CO2的物质的量为nmol,则CO2的变化物质的量为(1-n)mol,此时
>1,故此时平衡向逆反应移动,设平衡时CO2的物质的量为nmol,则CO2的变化物质的量为(1-n)mol,此时![]() =
=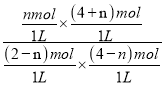 =1,解得n=0.8mol,即平衡时CO2的物质的量为0.8mol。
=1,解得n=0.8mol,即平衡时CO2的物质的量为0.8mol。

 天天练口算系列答案
天天练口算系列答案【题目】对四种金属G、L、M、R进行如下实验:
金属 实验 | G | L | M | R |
和冷水反应 | 无反应 | 慢慢反应 | 未做 | 未做 |
和2 mol/LHCl反应 | 溶解并放出气体 | 溶解并放出气体 | 无反应 | 无反应 |
和Rn+的水溶液反应 | 溶解并形成沉淀 | 未做 | 溶解并形成沉淀 | 未做 |
根据表中所给实验结果,判断这四种金属活泼性由强到弱的顺序正确的是
A. L、G、R、M B. G、L、M、R
C. L、G、M、R D. L、R、G、M