题目内容
【题目】结合图示实验装置,回答下列问题。
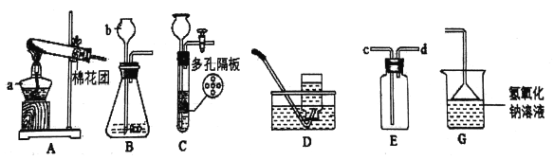
(1)指出图中b仪器的名称:b__________。
(2)用高锰酸钾固体制取氧气,若收集纯净的氧气,选用的收集装置是__________。实验室制取二氧化碳时,如需要E装置干燥二氧化碳,则E装置中应盛放__________,与B装置相比,若用C装置作为制取该气体的发生装置,其优点为__________。
(3)H2S是有毒气体,实验室常用块状硫化亚铁'(FeS)和稀H2SO4在常溫时发生反应制H2S,H2S气体的密度比空气大,易溶于水。
①实验室制H2S的化学方程式为__________。
②某同学用E装置来收集H2S气体应由__________端通入,另一端连接G装置。用G装置来处理H2S,其中漏斗的作用是__________。
【答案】 长颈漏斗 D 浓硫酸 可以控制反应的发生和停止 H2SO4+FeS=FeSO4+H2S↑ c 防止溶液倒吸
【解析】(1)依据实验室常用仪器的构造可知b为长颈漏斗;(2)加热高锰酸钾的方法制取氧气,据反应原理书写方程式:2KMnO4![]() K2MnO4+MnO2+O2↑;排水法收集的氧气较纯净,答案选D;硫酸具有吸水性,可用于干燥二氧化碳,实验室制取二氧化碳时,如需要E装置干燥二氧化碳,则E装置中应盛放浓硫酸;气体从c端进入;若用C装置(多孔隔板用来放块状固体)代替B装置为制取的发生装置,优点是:可以控制反应的发生和停止;(3)①硫化亚铁(FeS)和稀硫酸发生复分解反应生成硫酸亚铁和硫化氢,反应的方程式为:H2SO4+FeS=FeSO4+H2S↑;②H2S气体的密度比空气大,易溶于水,某同学用E装置来收集H2S气体由c通入;用G装置来收集处理H2S,因此漏斗的作用是防止溶液倒吸。
K2MnO4+MnO2+O2↑;排水法收集的氧气较纯净,答案选D;硫酸具有吸水性,可用于干燥二氧化碳,实验室制取二氧化碳时,如需要E装置干燥二氧化碳,则E装置中应盛放浓硫酸;气体从c端进入;若用C装置(多孔隔板用来放块状固体)代替B装置为制取的发生装置,优点是:可以控制反应的发生和停止;(3)①硫化亚铁(FeS)和稀硫酸发生复分解反应生成硫酸亚铁和硫化氢,反应的方程式为:H2SO4+FeS=FeSO4+H2S↑;②H2S气体的密度比空气大,易溶于水,某同学用E装置来收集H2S气体由c通入;用G装置来收集处理H2S,因此漏斗的作用是防止溶液倒吸。

【题目】下列实验操作或事实与预期实验目的或所得结论对应不正确的是
选项 | 实验操作或事实 | 实验目的或结论 |
A | 将滴有酚酞的氨水加热,红色逐渐变浅 | NH3·H2O受热分解,导致溶液碱性减弱 |
B | 在酒精灯上加热铝箔,铝箔熔化但不滴落 | Al2O3的熔点高于A1 |
C | 新收集的酸雨 | 酸雨中一定含有SO42- |
0 | 测同温同浓度Na2CO3和Na2SiO3水溶液的pH | 确定碳和硅两元素非金属性 |
A. A B. B C. C D. D
【题目】 氨是氮循环过程中的重要物质,氨的合成是目前普遍使用的人工固氮方法。
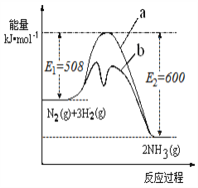
(1)根据下图提供的信息,写出该反应的热化学方程式
_____________________________________________,
下图的曲线中____________(填“a” 或“b”)表示 加入铁触媒(催化剂)的能量变化曲线。
(2)在恒容容器中,下列描述中能说明上述反应已达平衡的是_________________。
A.3υ(H2)正=2υ(NH3)逆
B.单位时间内生成n mol N2的同时生成2n molNH3
C.容器内气体的密度不随时间的变化而变化
D.容器内压强不随时间的变化而变化
(3)为了寻找合成NH3的适宜条件,某同学设计了三组实验(如下表),请在下表空格处填入相应的实验条件及数据。
实验编号 | T(℃) | n (N2)/n(H2) | P(MPa) |
ⅰ | 450 | 1/3 | 1 |
ⅱ | ______ | 1/3 | 10 |
ⅲ | 480 | ______ | 10 |
(4)合成氨的原料气氢气制备时其中一步反应: H2O(g)+CO(g)![]() CO2(g)+H2(g),在850 ℃时,其平衡常数K=1。若850 ℃时向体积为1 L的恒容密闭容器中,同时充入1.0 mol CO,3.0 mol H2O,1.0 mol CO2,5.0 mol H2,此时反应向____________(填“正反应”或“逆反应”)方向进行,平衡时CO2的物质的量为______________。
CO2(g)+H2(g),在850 ℃时,其平衡常数K=1。若850 ℃时向体积为1 L的恒容密闭容器中,同时充入1.0 mol CO,3.0 mol H2O,1.0 mol CO2,5.0 mol H2,此时反应向____________(填“正反应”或“逆反应”)方向进行,平衡时CO2的物质的量为______________。