题目内容
【题目】硫代硫酸钠(Na2S2O3)俗称保险粉,可用作照相定影剂、纸浆漂白脱氯剂等。
实验室可通过反应2Na2S+Na2CO3+4SO2→3Na2S2O3+CO2制取Na2S2O3,装置如图所示。
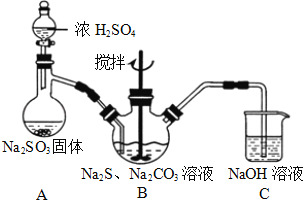
(1)装置B中搅拌器的作用是______;装置C中NaOH溶液的作用是_____。
(2)请对上述装置提出一条优化措施_______________________。
为测定所得保险粉样品中Na2S2O35H2O的质量分数,称取3.000g Na2S2O35H2O样品配成100mL溶液,用0.100mol/L标准碘溶液进行滴定,反应方程式为:2Na2S2O3+I2→2NaI+Na2S4O6
(3)滴定时用__________作指示剂,滴定时使用的主要玻璃仪器有________________。
(4)滴定时,若看到溶液局部变色就停止滴定,则样品中Na2S2O35H2O的质量分数测定值__________(填“偏高”、“偏低”或“不变”)。
(5)某学生小组测得实验数据如下:
实验次数 | 样品溶液体积(ml) | 滴定消耗0.100mol/L碘溶液体积(ml) |
1 | 20.00 | 9.80 |
2 | 20.00 | 10.70 |
3 | 20.00 | 9.90 |
该样品中Na2S2O35H2O的质量分数是_______。(精确到0.001)
【答案】 让反应物充分反应(或反应物充分混合或加快反应速度) 吸收二氧化硫尾气,防止空气污染 A中分液漏斗改为恒压漏斗,或者BC之间添加一个安全瓶防倒吸(合理即可) 淀粉 滴定管、锥形瓶 偏低 0.814
【解析】本题分析:本题主要考查氧化还原反应滴定的计算。
(1)装置B中搅拌器的作用是加快反应速度;装置C中NaOH溶液的作用是吸收二氧化硫尾气,防止空气污染。
(2)对上述装置提出的一条优化措施:A中分液漏斗改为恒压漏斗,或者BC之间添加一个安全瓶防倒吸。
(3)碘遇淀粉变蓝,滴定时用淀粉作指示剂,滴定时使用的主要玻璃仪器有滴定管、锥形瓶。
(4)滴定时,若看到溶液局部变色就停止滴定,这时Na2S2O3剩余,则样品中Na2S2O35H2O的质量分数测定值偏低。
(5)第2次实验数据不正常,弃去不用,剩余两次实验平均消耗0.100mol/L碘溶液9.85mL,该样品中Na2S2O35H2O的质量分数是(0.100mol L -1 ×0.00985mL ×2 ×248g/mol) ×5/3.000g =0.814 。