题目内容
【题目】控制适合的条件,将反应![]() 设计成如图所示的原电池。下列判断正确的是
设计成如图所示的原电池。下列判断正确的是
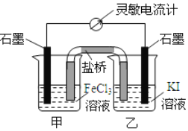
A. 反应开始时,甲中石墨电极上发生氧化反应
B. 反应开始时,乙中石墨电极上![]() 被还原
被还原
C. 电流计读数为零时,反应达到化学平衡状态,但反应还在进行
D. 电流计读数为零后,在甲中溶入![]() 固体,甲中石墨电极为正极
固体,甲中石墨电极为正极
【答案】C
【解析】
A.根据总方程式,FeCl3作正极,得到电子,发生还原反应,故A错误;
B. 因乙中I-失去电子放电,元素的化合价升高,则发生氧化反应,被氧化,故B错误;
C. 当电流计为零时,说明没有电子发生转移,则反应达到平衡,故C正确;
D. 当加入Fe2+,导致平衡逆向移动,则Fe2+失去电子生成Fe3+,作为负极,而乙中石墨成为正极,故D错误;
故选C。

练习册系列答案
相关题目
【题目】臭氧在烟气脱硝中的反应为2NO2(g)+O3(g)![]() N2O5(g)+O2(g)。若此反应在恒容密闭容器中进行,下列选项中有关图象对应的分析正确的是( )
N2O5(g)+O2(g)。若此反应在恒容密闭容器中进行,下列选项中有关图象对应的分析正确的是( )
A | B | C | D |
|
|
|
|
平衡后升温,NO2含量降低 | 0~2 s内,v(O3)=0.2 mol·L-1·s-1 | v正:b点>a点 b点:v逆>v正 | 恒温,t1时再充入O3 |
A. AB. BC. CD. D