题目内容
已知下列热化学方程式:
①CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l) ΔH1=-870.3 kJ/mol
②C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ/mol
③H2(g)+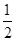 O2(g)===H2O(l) ΔH3=-285.8 kJ/mol
O2(g)===H2O(l) ΔH3=-285.8 kJ/mol
则反应④2C(s)+2H2(g)+O2(g)===CH3COOH(l)的焓变为
A.488.3 kJ/mol B.-224.15 kJ/mol
C.-488.3 kJ/mol D.244.15 kJ/mol
【答案】
C
【解析】
试题分析:利用盖斯定律:?×2+?×2-?=④,所以方程④的焓变△H=2×(-393.5 kJ/mol)+2×(-285.8 kJ/mol)-(-870.3 kJ/mol)=-488.3 kJ/mol,故选C
考点:热化学方程式、盖斯定律
点评:本题考查利用盖斯定律的计算,难度不大。

练习册系列答案
相关题目
 煤炭可以转化为清洁能源和化工原料.
煤炭可以转化为清洁能源和化工原料.