题目内容
【题目】下图表示溶液中c(H+)和c(OH﹣)的关系,下列判断错误的是
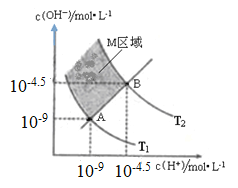
A. 两条曲线间任意点均有c(H+)×c(OH﹣)=KW
B. M区域内任意点均有c(H+)<c(OH﹣)
C. 图中T1<T2
D. XZ线上任意点均有pH=7
【答案】D
【解析】
A.依图可知,曲线上的任意点均是平衡点,且温度一定,所以其水的离子积是一个常数,故A正确;
B.当c(H+)=10-7mol/L时,向上做垂线得在M区域内c(OH-)>10-7mol/L,故B正确;C.水的电离是吸热反应,升高温度促进水的电离,c(H+)、c(OH-)及Kw都增大,所以T2>T1,故C正确;
D.XZ线上任意点表示溶液呈中性,由于各点温度不同,故PH不同,故D项错误。
故选D。

 全能闯关100分系列答案
全能闯关100分系列答案【题目】实施以节约能源和减少废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择。化工行业的发展必须符合国家节能减排的总体要求。试运用所学知识,回答下列问题:
(1)已知某温度下某反应的化学平衡常数表达式为:K=c(H2O)/[ c(CO)·c(H2)]所对应的化学反应方程式为:________。
(2)已知在一定温度下:
①C(s)+CO2(g) ![]() 2CO(g) △H1=a kJ/mol 平衡常数K1;
2CO(g) △H1=a kJ/mol 平衡常数K1;
②CO(g)+H2O(g) ![]() H2(g)+CO2(g) △H2=b kJ/mol 平衡常数K2;
H2(g)+CO2(g) △H2=b kJ/mol 平衡常数K2;
③C(s)+H2O(g) ![]() CO(g)+H2(g)△H3 平衡常数K3。
CO(g)+H2(g)△H3 平衡常数K3。
则K1、K2、K3之间的关系是:________,△H3=________(用含a、b的代数式表示)。
(3)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题。已知等体积的一氧化碳和水蒸气进入反应器时,发生如下反应:CO(g)+H2O(g) ![]() H2(g)+CO2(g),该反应平衡常数随温度的变化如下表所示:
H2(g)+CO2(g),该反应平衡常数随温度的变化如下表所示:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
该反应的正反应方向是________反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020 mol/L,在该条件下,CO的平衡转化率为:________。