题目内容
【题目】探究新制饱和氯水成分的实验时,由实验现象得出的结论错误的是
A.氯水呈浅黄绿色,说明氯水中含有Cl2
B.向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含Cl-
C.向氯水中滴加NaHCO3,有气泡产生,说明氯水中含有HCl和HClO
D.向FeCl2溶液中滴加氯水,溶液变成棕黄色,说明氯水中含有HClO
【答案】CD
【解析】
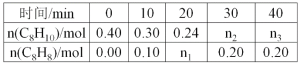
A.氯气为黄绿色气体,氯水的颜色呈浅绿色,说明氯水中含有![]() ,A正确;
,A正确;
B.向氯水中滴加硝酸酸化的![]() 溶液,产生白色沉淀,说明氯水中含有
溶液,产生白色沉淀,说明氯水中含有![]() ,B正确;
,B正确;
C.向氯水中加入![]() 粉末,有二氧化碳产生,说明氯水中含有HCl,HClO酸性比碳酸弱,不能和
粉末,有二氧化碳产生,说明氯水中含有HCl,HClO酸性比碳酸弱,不能和![]() 反应生成二氧化碳,C错误;
反应生成二氧化碳,C错误;
D.向![]() 溶液中滴加氯水,溶液颜色变成棕黄色,氯水中氯分子可以氧化亚铁离子,D错误。
溶液中滴加氯水,溶液颜色变成棕黄色,氯水中氯分子可以氧化亚铁离子,D错误。
答案选CD。

【题目】实验小组以二氧化锰和浓盐酸为反应物,连接装置A→B→C制取氯水,并探究氯气和水反应的产物。
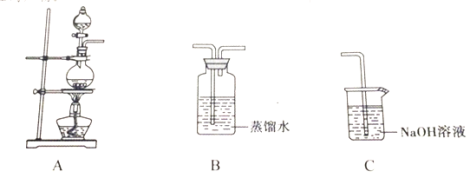
(1)A中发生反应的离子方程式是_________。
(2)B中得到浅黄绿色的饱和氯水,将所得氯水分三等份,进行的操作、现象、结论如下:
实验 | 实验操作 | 现象 | 结论 |
Ⅰ | 向氯水中加入碳酸氢钠粉末 | 有无色气泡产生 | 氯气与水反应至少产生了一种酸性强于碳酸的物质 |
Ⅱ | 向品红溶液中滴入氯水 | 溶液褪色 | 氯气与水反应的产物有漂白性 |
(1)甲同学指出:由实验Ⅰ得出的结论不合理,原因是制取的氯水中含有杂质______(填化学式),也能与碳酸氢钠反应产生气泡。应在A、B间连接除杂装置,请画出除杂装置并标出气体流向和药品名称______。
(2)乙同学指出由实验Ⅱ得出的结论不合理,原因是实验未证明_______(填化学式)是否有漂白性。
(3)丙同学利用正确的实验装置发现氯水中有Cl-存在,证明氯水中有Cl-的操作和现象是:_____。丙同学认为,依据上述现象和守恒规律,能推测出氯水中有次氯酸存在。这一推测是否正确,请说明理由________。
(4)丁同学利用正确的实验装置和操作进行实验,观察到实验现象与实验Ⅰ、Ⅱ相似,说明氯气和水反应的产物具有的性质是________。
(5)戊同学将第三份氯水分成两等份,向其中一份加入等体积的蒸馏水,溶液接近无色。另一份中加入等体积饱和的氯化钠溶液,溶液为浅黄绿色。对比这两个实验现象能说明:_______。