题目内容
【题目】某温度时,在一个容积为2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
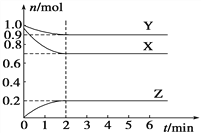
(1)该反应的化学方程式为_______________;
(2)反应开始至2 min,气体Z的反应速率为_________;
(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的________倍;
②若此时将容器的体积缩小为原来的 0.5倍,达到平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应的正反应为______反应(填“放热”或“吸热”)。
(4)若X为固体、Y、Z为气体,则该反应的平衡常数表达式为__________________。
【答案】 3X+Y![]() 2Z 0.05 mol·L-1·min-1 0.9 吸热 K =c2(Z)/ c(Y)
2Z 0.05 mol·L-1·min-1 0.9 吸热 K =c2(Z)/ c(Y)
【解析】(1). 据图可知,在该反应中X、Y的物质的量减小,Z的物质的量增大,则X、Y为反应物,Z为生成物,且△n(X):△n(Y):△n(Z)=0.3mol:0.1mol:0.2mol=3:1:2,则该反应的化学方程式为:3X+Y![]() 2Z,故答案为:3X+Y
2Z,故答案为:3X+Y![]() 2Z;
2Z;
(2). 反应开始至2 min时,用气体Z表示的反应速率为v(Z)= 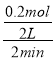 =0.05 mol·L-1·min-1,故答案为:0.05 mol·L-1·min-1;
=0.05 mol·L-1·min-1,故答案为:0.05 mol·L-1·min-1;
(3). ①. 若X、Y、Z均为气体,在同温同体积的密闭容器中,反应达到平衡时的压强与反应开始时的压强之比等于平衡时气体总物质的量与反应开始时气体总物质的量之比,据图可知,反应开始时气体总物质的量为2mol,达到平衡时气体总物质的量为(0.9+0.7+0.2)mol=1.8mol,则: ![]() =
=![]() =
=![]() =0.9,故答案为:0.9;
=0.9,故答案为:0.9;
②. 由反应3X+Y![]() 2Z可知,该反应为气体物质的量减少的可逆反应,将容器的体积缩小为原来的 0.5倍,容器的压强增大,平衡正向移动,此时容器内温度降低,说明正反应为吸热反应,故答案为:吸热;
2Z可知,该反应为气体物质的量减少的可逆反应,将容器的体积缩小为原来的 0.5倍,容器的压强增大,平衡正向移动,此时容器内温度降低,说明正反应为吸热反应,故答案为:吸热;
(4). 若X为固体、Y、Z为气体,则反应3X+Y![]() 2Z的平衡常数表达式为:K=c2(Z)/ c(Y),故答案为:K=c2(Z)/ c(Y)。
2Z的平衡常数表达式为:K=c2(Z)/ c(Y),故答案为:K=c2(Z)/ c(Y)。

 阅读快车系列答案
阅读快车系列答案