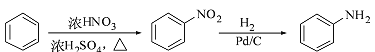
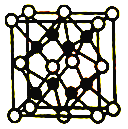
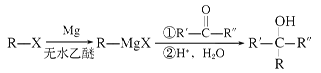题目内容
【题目】苹果酸的结构简式为:![]() ,易溶于水,下列说法正确的是( )
,易溶于水,下列说法正确的是( )
A. 1 mol苹果酸可与3 mol NaOH发生中和反应
B. 苹果酸的一种缩聚产物是![]()
C. 含1 mol苹果酸的稀溶液与足量金属Na反应生成1.5 mol H2
D. 苹果酸的催化氧化产物能发生银镜反应
【答案】B
【解析】A、苹果酸中含有羧基和羟基,能与NaOH反应的官能团是羧基,1mol苹果酸中含有2mol羧基,能与2molNaOH发生中和反应,故A错误;B、发生类似与酯化反应,羧基去掉羟基,羟基去掉氢,即缩聚产物为![]() 和
和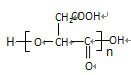 ,故B正确;C、苹果酸溶液中含有水,加入足量的金属钠,不仅与羧基、羟基发生反应产生氢气,而且还与水反应产生氢气,产生氢气的物质的量大于1.5mol,故C错误;D、苹果酸催化氧化产物是:
,故B正确;C、苹果酸溶液中含有水,加入足量的金属钠,不仅与羧基、羟基发生反应产生氢气,而且还与水反应产生氢气,产生氢气的物质的量大于1.5mol,故C错误;D、苹果酸催化氧化产物是: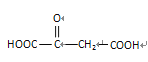 ,不含醛基,不能与银氨溶液反应,故D错误。
,不含醛基,不能与银氨溶液反应,故D错误。

 中考解读考点精练系列答案
中考解读考点精练系列答案【题目】碘及其化合物在科研、生活等方面有广泛用途。回答下列问题:
(1)海带中富含碘,按如下实验流程可对海带中碘的含量进行测定。

取0.0100 mol/L的AgNO3标准溶液装入棕色滴定管,取100.00 mL海带浸取原液至滴定池,用电势滴定法测定碘含量。测得的电动势(E) 反映溶液中c(Iˉ)的变化,部分数据如下表:
V(AgNO3)/mL | 15.00 | 19.00 | 19.80 | 19.98 | 20.00 | 20.02 | 21.00 | 23.00 | 25.00 |
E/mV | -225 | -200 | -150 | -100 | 50.0 | 175 | 275 | 300 | 325 |
①灼烧海带时,除需要坩埚外,还需要用到的实验仪器是____________ (填序号)。
a.烧杯 b.三脚架 c.温度计 d.泥三角 e.酒精灯 f.坩埚钳
②使用棕色滴定管的原因是_____________________。
③根据表中数据,计算海带中碘的百分含量为____________。
(2)“大象的牙膏”是著名化学实验之一,其实验方法是将浓缩的过氧化氢溶液与肥皂液混合,再滴加少量碘化钾溶液,即可观察到泡沫状物质像喷泉一样喷涌而出。
已知:2H2O2(l)=2H2O(l)+O2(g) △H=-196kJ/mol,活化能Ea=76kJ/mol,若用I-催化时活化能Ea’=57kJ/mol。
①在H2O2溶液中加入KI溶液作催化剂,反应过程中发生I-与IO-之间的转化,请依次写出发生反应的离子方程式:
反应甲:______________________;
反应乙:______________________。
②反应甲为吸热反应,且甲的反应速率小于乙的反应速率,在下图中画出在H2O2溶液中加入KI后,反应过程的能量变化图。_______

(3)HI不稳定,其水溶液具有强酸性。现用0.lmol/LKI溶液、NH4I固体、pH试纸设计实验验证上述性质。简述实验方案。
①强酸性:__________________________。
②不稳定性:___________________________。