题目内容
【题目】某研究小组用如图装置进行SO2与FeCl3溶液反应的相关实验(夹持装置已略去)。
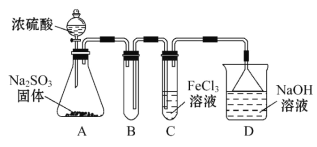
(1)通入足量SO2时C中观察到的现象为_____________________________。
(2)根据以上现象,该小组同学认为SO2与FeCl3溶液发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式______________________________;
②请设计实验方案检验有Fe2+生成_________________________。
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42-。该做法_______(填“合理”或“不合理”),理由是____________
(3)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有________(填序号)。
A.浓硫酸 B.酸性KMnO4溶液 C.碘水 D.NaCl溶液
【答案】溶液由棕黄色变成浅绿色 2Fe3+ + SO2 +2H2O=SO42-+4H+ +2Fe2+ 取少量C中反应后的溶液于试管中,向其中滴入酸性KMnO4溶液,若褪色说明有Fe2+,不褪色说明没有Fe2+ 不合理 HNO3可以将SO2氧化成H2SO4,干扰实验 BC
【解析】
(1)利用Fe3+具有强氧化性,C中发生离子方程式为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,Fe3+显棕黄色,Fe2+显浅绿色,现象为溶液由棕黄色变成浅绿色;
(2)①根据上述分析,发生离子方程式为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+;
②Fe2+以还原性为主,检验Fe2+实验方案是 取少量C中反应后的溶液于试管中,向其中滴入酸性KMnO4溶液,若褪色说明有Fe2+,不褪色说明没有Fe2+;
③HNO3具有强氧化性,能把SO2氧化成H2SO4,干扰实验,因此该做法不合理;
(3)A、浓硫酸与SO2不发生反应,浓硫酸不能代替FeCl3,故A不符合题意;
B、酸性高锰酸钾溶液具有强氧化性,如果紫红色褪去,说明SO2具有还原性,故B符合题意;
C、碘水中I2,具有强氧化性,能把SO2氧化,淡黄色褪去,说明SO2具有还原性,故C符合题意;
D、NaCl溶液不与SO2发生反应,不能鉴别SO2有还原性,故D不符合题意。

 备战中考寒假系列答案
备战中考寒假系列答案【题目】某温度下,H2(g) + CO2(g) ![]() H2O(g)+ CO(g)的平衡常数K=9/4。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和 CO2(g),其起始浓度如下表所示
H2O(g)+ CO(g)的平衡常数K=9/4。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和 CO2(g),其起始浓度如下表所示
起始浓度 | 甲 | 乙 | 丙 |
C(H2)/ mol·l-1 | 0.010 | 0.020 | 0.020 |
C(CO2)/ mol·l-1 | 0.010 | 0.010 | 0.020 |
下列判断不正确的是
A. 平衡时,乙中CO2 的转化率大于60%
B. 平衡时,甲和丙中H2 的转化率均是60%
C. 平衡时,丙中C(CO2)是甲中的2倍,是0.012 mol·l-1
D. 反应开始时,丙中的反应速率最快,甲中的反应速率最慢