题目内容
7.425℃时,在1L密闭容器中进行的反应:H2+I2=2HI达到平衡,分别说明下列各图所表示的含义.由图中的事实可以说明化学平衡具有哪些特征?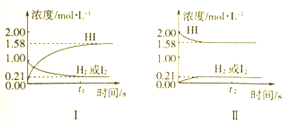
分析 根据图Ⅰ可以看出,H2和I2逐渐减小直到不变,而HI逐渐增大直到不变,图Ⅱ可以看出,HI逐渐减小直到不变,而H2和I2逐渐增大直到不变,据此分析.
解答 解:根据图Ⅰ可以看出,H2和I2逐渐减小直到不变,而HI逐渐增大直到不变,图Ⅱ可以看出,HI逐渐减小直到不变,而H2和I2逐渐增大直到不变,由此可以说明化学平衡具有动、等、定、变等特征,答:化学平衡具有动、等、定、变等特征.
点评 本题主要考查了平衡的特征,难度不大,注意基础知识的积累.

练习册系列答案
相关题目
17.能正确表示下列反应的离子反应方程式为( )
| A. | NH4HCO3溶于过量的浓KOH溶液中:NH4++HCO3-+2OH-=CO32-+NH3↑+2H2O | |
| B. | 向明矾溶液中滴加Ba(OH)2溶液,使沉淀质量达到最大值:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ | |
| C. | 钠与水的反应:Na+2H2O=Na++2OH-+H2↑ | |
| D. | 硫酸氢钠溶液与足量氢氧化钡溶液混合:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
18.下列的各组离子在酸性溶液中能大量共存的是( )
| A. | Na+、Fe2+、NO3-、Cl- | B. | Ca2+、K+、Cl-、NO3- | ||
| C. | Al3+、K+、OH-、NO3- | D. | Na+、Ca2+、SiO32-、Cl- |
15.在NaHSO4溶液中离子的总浓度为0.06mol/L,若加入等体积离子浓度为0.06mol/L的Ba(OH)2溶液,混合后溶液的体积不变,则溶液的pH值为( )
| A. | 2 | B. | 1.7 | C. | 12 | D. | 12.3 |
2.下列物质的水溶液经加热浓缩、蒸干灼烧后仍能得到原物质的是( )
| A. | AlCl3 | B. | Ca(HCO3)2 | C. | NaAlO2 | D. | Na2SO3 |
19.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,22.4 L Cl2中含有的分子数为NA | |
| B. | 32g O2和O3的混合气体中含有的O原子数为2NA | |
| C. | 1mol/L AlCl3溶液中含有铝离子的个数为3NA | |
| D. | 5.6g Fe与足量稀硝酸反应失去的电子数为0.2 NA |
16.下列物质互为同位素的是( )
| A. | H2和D2 | B. | 金刚石和石墨 | ||
| C. | CO和CO2 | D. | ${\;}_{17}^{37}$Cl和${\;}_{17}^{35}$Cl |
17.下列各组物质中,一定量的气体X和一定量的气体Y同时通入盛有溶液Z的洗气瓶中,最终肯定有沉淀生成的是(空气不参与反应)( )
| A. | X-NH3 Y-SO2 Z-BaCl2 | B. | X-NO2 Y-SO2 Z-BaCl2 | ||
| C. | X-HCl Y-CO2 Z-Ca(OH)2 | D. | X-CO2 Y-SO2 Z-CaCl2 |
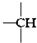 、
、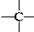 ,其数目分别用a、b、c、d表示,对烷烃(除甲烷外)中存在的关系作讨论:
,其数目分别用a、b、c、d表示,对烷烃(除甲烷外)中存在的关系作讨论: