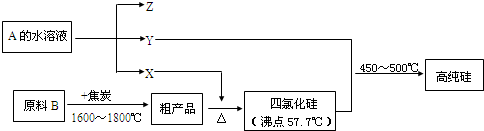
题目内容
12.下列说法不正确的是( )| A. | 化学反应除了生成新物质外,还伴随着能量的变化 | |
| B. | 放热反应都不需要加热就能发生 | |
| C. | 吸热反应在一定条件(如常温、加热等)也能发生 | |
| D. | 化学反应是放热还是吸热,取决于生成物具有的总能量和反应物具有的总能量的大小 |
分析 A.化学变化是生成新物质的变化,除有新物质生成外,能量的变化也必然发生,从外观检测往往为温度的变化,即常以热量的变化体现;
B.放热的化学反应,如燃烧需要达到着火点;
C.有的吸热反应,不需要加热也能发生;
D.反应的能量变化取决于反应物和生成物能量高低.
解答 解:A.化学反应的本质是有新物质的生成,生成新化学键所释放的能量与断裂旧化学键所吸收的能量不等,所以化学反应除了生成新的物质外,还伴随着能量的变化,故A正确;
B.放热反应有的需加热,如木炭的燃烧是一个放热反应,但需要点燃,点燃的目的是使其达到着火点,故B错误;
C.Ba(OH)2•8H2O与NH4Cl的反应是吸热反应,但不需要加热,故C正确;
D.化学反应放热还是吸热,取决于生成物具有的总能量和反应物具有的总能量,依据能量守恒分析判断反应能量变化,故D正确;
故选B.
点评 本题考查化学反应的能量变化的定性判断,一个反应是吸热还是放热,关键在于相对能量的大小.

练习册系列答案
相关题目
2.关于有机物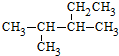 的系统命名正确的是( )
的系统命名正确的是( )
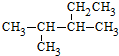 的系统命名正确的是( )
的系统命名正确的是( )| A. | 2-甲基-3-乙基丁烷 | B. | 3-甲基-2-乙基丁烷 | ||
| C. | 2,3-二甲基戊烷 | D. | 3,4-二甲基戊烷 |
3.人体内存在着酸碱平衡,如出现失衡将对人体健康产生极大危害.人体内生成的下列酸属于无机物的是( )
| A. | 乳酸(C3H6O3) | B. | 磷酸(H3PO4) | C. | 丙酮酸(C3H4O3) | D. | 乙酰乙酸(C4H6O3) |
20.有下列物质:①甲烷 ②丙烷 ③戊烷 ④2-甲基丁烷 ⑤2,2-二甲基丙烷,它们的沸点排列顺序正确的是( )
| A. | ①>②>③>④>⑤ | B. | ③>④>⑤>②>① | C. | ⑤>④>③>②>① | D. | ②>①>⑤>④>③ |
7.下列各组物质中,肯定全都属于纯净物的是( )
| A. | 液氯和氯水 | B. | 酒精溶液和乙醇 | ||
| C. | 七水合硫酸亚铁和硫酸亚铁 | D. | 干冰和混有冰的干冰 |
17.进行化学实验必须注意安全,下列说法不正确的是( )
| A. | 为防止试管破裂,加热固体时试管口一般要略高于试管底 | |
| B. | 不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液 | |
| C. | 不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 | |
| D. | 酒精灯着火时用湿抹布盖灭 |
2.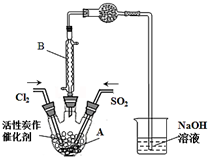 某学习小组依据反应:SO2(g)+Cl2(g?SO2Cl2(g)△H<0,设计制备磺酰氯(SO2Cl2)的装置如图,有关信息如表所示.
某学习小组依据反应:SO2(g)+Cl2(g?SO2Cl2(g)△H<0,设计制备磺酰氯(SO2Cl2)的装置如图,有关信息如表所示.
(1)若用浓盐酸与二氧化锰为原料制取Cl2,反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(2)B仪器的作用是使挥发的产物SO2Cl2冷凝回流.
(3)为了便于混合物的分离且提高反应物的转化率,A装置的反应条件最好选择a.
a.冰水浴 b.常温 c.加热至69.1℃
(4)如果通入的Cl2或SO2含有水蒸气,氯气和二氧化硫可能发生反应的化学方程式为SO2+Cl2+2H2O═H2SO4+2HCl.
(5)实验时先通入干燥的Cl2将A装置中的空气赶走,再缓慢通入干燥的SO2,即发生反应.充分反应后,继续通入Cl2使装置中的SO2进入烧杯中被吸收.分离产物后,向获得的SO2Cl2中加水,出现白雾,振荡、静置得到无色溶液W.
①经分析SO2Cl2与H2O反应属于非氧化还原反应,写出该反应的化学方程式SO2Cl2+2H2O=H2SO4+2HCl.
②无色溶液W中的阴离子除含少量OH-外,还含有其它两种阴离子,检验溶液W中这两种阴离子方法是取少量W溶液于试管中,加入过量Ba(NO3)2溶液,有不溶于稀硝酸的白色沉淀产生,说明溶液中含有SO42-,过滤,向滤液中滴加HNO3酸化,再加入AgNO3溶液,产生白色沉淀,则说明溶液中有Cl-.
③反应完成后,在W溶液、烧杯中分别滴加过量的BaCl2溶液,均出现白色沉淀,此沉淀不溶于稀盐酸,经过滤、洗涤、干燥,称量得到的固体质量分别为xg、yg.计算SO2+Cl2?SO2Cl2反应中,SO2的转化率$\frac{X}{X+Y}$×100%(用含x、y的代数式表示).
 某学习小组依据反应:SO2(g)+Cl2(g?SO2Cl2(g)△H<0,设计制备磺酰氯(SO2Cl2)的装置如图,有关信息如表所示.
某学习小组依据反应:SO2(g)+Cl2(g?SO2Cl2(g)△H<0,设计制备磺酰氯(SO2Cl2)的装置如图,有关信息如表所示.| SO2Cl2 | Cl2 | SO2 | |
| 熔点/℃ | -54.1 | -101 | -72.4 |
| 沸点/℃ | 69.1 | -34.6 | -10 |
| 性质 | 遇水发生剧烈 |
(2)B仪器的作用是使挥发的产物SO2Cl2冷凝回流.
(3)为了便于混合物的分离且提高反应物的转化率,A装置的反应条件最好选择a.
a.冰水浴 b.常温 c.加热至69.1℃
(4)如果通入的Cl2或SO2含有水蒸气,氯气和二氧化硫可能发生反应的化学方程式为SO2+Cl2+2H2O═H2SO4+2HCl.
(5)实验时先通入干燥的Cl2将A装置中的空气赶走,再缓慢通入干燥的SO2,即发生反应.充分反应后,继续通入Cl2使装置中的SO2进入烧杯中被吸收.分离产物后,向获得的SO2Cl2中加水,出现白雾,振荡、静置得到无色溶液W.
①经分析SO2Cl2与H2O反应属于非氧化还原反应,写出该反应的化学方程式SO2Cl2+2H2O=H2SO4+2HCl.
②无色溶液W中的阴离子除含少量OH-外,还含有其它两种阴离子,检验溶液W中这两种阴离子方法是取少量W溶液于试管中,加入过量Ba(NO3)2溶液,有不溶于稀硝酸的白色沉淀产生,说明溶液中含有SO42-,过滤,向滤液中滴加HNO3酸化,再加入AgNO3溶液,产生白色沉淀,则说明溶液中有Cl-.
③反应完成后,在W溶液、烧杯中分别滴加过量的BaCl2溶液,均出现白色沉淀,此沉淀不溶于稀盐酸,经过滤、洗涤、干燥,称量得到的固体质量分别为xg、yg.计算SO2+Cl2?SO2Cl2反应中,SO2的转化率$\frac{X}{X+Y}$×100%(用含x、y的代数式表示).