题目内容
1.某同学想探究S03与Na0H能否发生反应,请你帮他完成方案设计:将S03与少量的酚酞和氢氧化钠溶液混合;若出现溶液红色消失现象.则说明反应能够发生.分析 氢氧化钠溶液显碱性,与酚酞混合溶液为红色,把S03与少量的酚酞和氢氧化钠混合溶液反应,根据现象判断.
解答 解:氢氧化钠溶液显碱性,与酚酞混合溶液为红色,把S03与少量的酚酞和氢氧化钠混合溶液反应,若溶液红色消失,说明NaOH被消耗,即S03与Na0H发生了反应;
故答案为:酚酞和氢氧化钠;溶液红色消失.
点评 本题考查了三氧化硫和氢氧化钠的性质,题目难度不大,侧重于考查元素化合物的性质,考查了学生的实验探究能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.下列说法中不正确的是( )
| A. | 根据某种原子的质量数可以确定该元素的相对原子质量 | |
| B. | H-N=C=O与H-O-C≡N互为同分异构体 | |
| C. | 化学键存在于化合物中,也可能存在于单质中 | |
| D. | 35Cl与37Cl是两种不同的核素 |
6.对于可逆反应mA(g)+nB(g)?C(s)+qD(g)反应过程中,其他条件不变时,产物D的质量分数D%与温度T或压强P的关系如图所示,请判断下列说法正确的是( )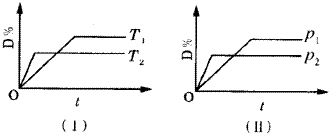

| A. | 降温,化学平衡向正反应方向移动 | |
| B. | 使用催化剂可使%有所增加 | |
| C. | 化学方程式中气体的化学计量数m+n>q | |
| D. | B的颗粒越小,正反应速率越快,有利于平衡向正反应方向移动 |
10.下列粒子在反应中只能作氧化剂的是( )
| A. | O 2- | B. | Cl 2 | C. | HCl | D. | Fe 3+ |
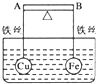 如图杠杆AB两端分别挂着体积相同、质量相同的空心铁球和空心铜球.调节杠杆使其保持平衡,一段时间后小心加入浓CuSO4溶液,回答下列有关问题(不考虑铁丝反应和两球的浮力变化)
如图杠杆AB两端分别挂着体积相同、质量相同的空心铁球和空心铜球.调节杠杆使其保持平衡,一段时间后小心加入浓CuSO4溶液,回答下列有关问题(不考虑铁丝反应和两球的浮力变化)