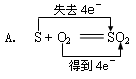
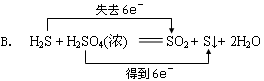
题目内容
对单质铁溶于稀硝酸的过程如下分析:
(1)当发生的反应Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O时,n(HNO3)与n(Fe)的大小关系为 。(n表示物质的量)
(2)当n(HNO3)≤8n(Fe)/3时,发生反应的离子方程式为
(3)当8n(Fe)/3<n(HNO3)<4n(Fe)时,发生的反应可表示为aFe+bHNO3(稀)=cNO↑+dFe(NO3)2+eFe(NO3)3+fH2O。
现假设a=16,且b、c、d、e、f均为整数,可得到多组化学计量数(系数)的配比,请将它们填入下表(可不填满,也可以补充):
(1)当发生的反应Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O时,n(HNO3)与n(Fe)的大小关系为 。(n表示物质的量)
(2)当n(HNO3)≤8n(Fe)/3时,发生反应的离子方程式为
(3)当8n(Fe)/3<n(HNO3)<4n(Fe)时,发生的反应可表示为aFe+bHNO3(稀)=cNO↑+dFe(NO3)2+eFe(NO3)3+fH2O。
现假设a=16,且b、c、d、e、f均为整数,可得到多组化学计量数(系数)的配比,请将它们填入下表(可不填满,也可以补充):
| 组次 | a | B | c | d | e | f |
| 一 | 16 | | 11 | | | 22 |
| 二 | 16 | | | | | |
| 三 | 16 | | | | | |
| 四 | 16 | | | | | |
| 五 | 16 | | | | | |
| 六 | | | | | | |
(1)n(HNO3)≥4n(Fe) (2)3Fe+8H++2NO3-=3Fe2++2NO+4H2O
(3)
(3)
| 组次 | a | B | c | d | e | f |
| 一 | 16 | 44 | 11 | 15 | 1 | 22 |
| 二 | 16 | 48 | 12 | 12 | 4 | 24 |
| 三 | 16 | 52 | 13 | 9 | 7 | 26 |
| 四 | 16 | 56 | 14 | 6 | 10 | 28 |
| 五 | 16 | 60 | 15 | 3 | 13 | 30 |
| 六 | 16 | | | | | |
(1)根据方程式可知,要生成硝酸铁,则硝酸必须是过量的,即n(HNO3)≥4n(Fe)。
(2)如果铁过量,则发生反应2Fe(NO3)3+Fe=3Fe(NO3)2,所以当n(HNO3)≤8n(Fe)/3时,发生反应的离子方程式为3Fe+8H++2NO3-=3Fe2++2NO+4H2O。
(3)本题在进行计算时,应该遵循原子守恒和电荷守恒。即d+e=a、2d+3e=3c、b=c+2d+3e、b=2f、3b=c+6d+9e。
(2)如果铁过量,则发生反应2Fe(NO3)3+Fe=3Fe(NO3)2,所以当n(HNO3)≤8n(Fe)/3时,发生反应的离子方程式为3Fe+8H++2NO3-=3Fe2++2NO+4H2O。
(3)本题在进行计算时,应该遵循原子守恒和电荷守恒。即d+e=a、2d+3e=3c、b=c+2d+3e、b=2f、3b=c+6d+9e。

练习册系列答案
相关题目
 2MoO3+4SO2 ②MoO3+2NH3·H2O=(NH4)2MoO4+H2O
2MoO3+4SO2 ②MoO3+2NH3·H2O=(NH4)2MoO4+H2O 4H++2Fe2++________;
4H++2Fe2++________;