题目内容
【题目】I.某化学课外小组用如右图一装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
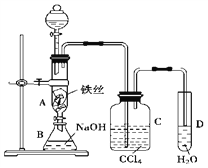
(1)观察到A中的现象是_________________。
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡, 写出有关反应的化学方程式 _________________。
(3)C中盛放CCl4的作用是_____________________________________________。
(4)若证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是 ______________________________。
II.实验室制备硝基苯的主要步骤如下:①配制一定比例的浓硫酸与浓硝酸的混合酸,加入反应器中;②向室温下的混合酸中逐滴加入一定量的苯,充分振荡,混合均匀;③在50~60℃下发生反应,直至反应结束;④除去混合酸后,粗产品依次用蒸馏水和5%NaOH溶液洗涤,最后再用蒸馏水洗涤;⑤将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯净的硝基苯。 请填写下列空白:
(1)配制一定比例浓硫酸和浓硝酸混合酸时,正确操作是___________________________。
(2)步骤③中,为了使反应在50~60℃下进行,常用的方法是_________________________。
(3)步骤④中粗产品用5%NaOH溶液洗涤的目的是 _________________________________。
【答案】 反应液微沸,有红棕色气体充满A容器 Br2+2NaOH==NaBr+NaBrO+H2O 除去溴化氢气体中的溴蒸气 石蕊试液;溶液变红色 先将浓硝酸注入容器中,再慢慢注入浓硫酸,并及时搅拌和冷却 将反应器放在50~60℃(或60℃)的水浴中加热 除去粗产品中残留的酸
【解析】I、(1)溴与铁反应生成溴化铁,反应现象为:反应液微沸有红棕色气体充满A容器。
故答案为:反应液微沸有红棕色气体充满A容器;
(2)实验结束后,打开A下端活塞,将反应后的溶液流入NaOH溶液中,NaOH可以与剩余的溴发生反应,以除去溴苯中的溴,反应方程式:Br2+2NaOH═NaBr+NaBrO+H2O;
故答案为:Br2+2NaOH═NaBr+NaBrO+H2O;
(3)CCl4能溶解挥发出的Br2,不能溶解HBr,故C中CCl4的作用是:除去溴化氢气体中的溴蒸气;
故答案为:除去溴化氢气体中的溴蒸气;
(4)如果苯和液溴发生的是取代反应,则有HBr生成,如果发生的是加成反应,则无HBr生成。也就是说,如果要证明苯和液溴发生的是取代反应,而不是加成反应,只需检验有无HBr生成,溴化氢与硝酸银反应生成溴化银淡黄色沉淀或在D中加入石蕊试液,若变红则发生取代反应。
故答案为:石蕊试液;溶液变红色.
II、(1)浓硫酸与浓硝酸混合放出大量的热,配制混酸操作注意事项是:先将浓硝酸注入容器中,再慢慢注入浓硫酸,并及时搅拌和冷却。
故答案为:先将浓硝酸注入容器中,再慢慢注入浓硫酸,并及时搅拌和冷却;
(2)由于控制温度50-60℃,应采取50~60℃水浴加热。
故答案为:采取50~60℃水浴加热;
(3)反应得到粗产品中有残留的硝酸及硫酸,用NaOH溶液洗涤除去粗产品中残留的酸。
故答案为:除去粗产品中残留的酸。

 名校课堂系列答案
名校课堂系列答案