题目内容
【题目】化学实验是化学学习的重要内容。根据你掌握的知识,完成下面内容。
(1)实验室需要1mol·L-1NaOH溶液245mL,请回答下列问题:
①为了配制此溶液应选择____mL的容量瓶,用天平称取____g NaOH。
②溶解NaOH后的溶液需冷却到室温后方能转移入容量瓶中。若趁热转移会使溶液的浓度____(填“偏大”或“偏小”,下同);在洗涤烧杯和玻璃棒的过程中,每次洗涤液均需注入容量瓶,洗涤液若不转移入容量瓶,会导致溶液的浓度____。
③当溶质完全转移至容量瓶后,需要确定溶液的容积,我们称之为定容。定容时,先直接加水至刻度下1~2cm处,改用___加水至溶液凹液面与刻度线相切。
(2)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取分液 B.升华 C.结晶 D.过滤 E.蒸馏 F.分液
①分离饱和食盐水与沙子的混合物____;
②从碘水中提取碘单质____;
③分离水和汽油的混合物___;
④分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物___。
【答案】250 10.0 偏大 偏小 胶头滴管 D A F E
【解析】
(1)①依据配制溶液体积选择合适容量瓶,依据m=cVM计算需要溶质的质量;
②依据c=![]() 进行误差分析;
进行误差分析;
③定容要用胶头滴管进行;
(2)①沙子不溶于水;
②碘不易溶于水,易溶于有机溶剂;
③水和汽油分层;
④CCl4和甲苯互溶,但沸点不同.
(1)①实验室需要1mol·L-1 NaOH溶液245mL,为了配制此溶液应选择250mL的容量瓶,用天平称取m=1mol·L-1×0.25L×40g·mol-1=10.0g NaOH;
②溶解NaOH后的溶液需冷却到室温后方能转移入容量瓶中,若趁热转移会使溶液的浓度,导致溶液体积偏小,依据c=![]() 可知溶液浓度偏大;
可知溶液浓度偏大;
在洗涤烧杯和玻璃棒的过程中,每次洗涤液均需注入容量瓶,洗涤液若不转移入容量瓶,会导致溶液的浓度,导致溶质的物质的量偏小,依据c=![]() ,导致溶液浓度偏小;
,导致溶液浓度偏小;
③当溶质完全转移至容量瓶后,需要确定溶液的容积,我们称之为定容;定容时,先直接加水至刻度下1~2cm处,改用胶头滴管加水至溶液凹液面与刻度线相切;
(2)①分离饱和食盐水与沙子的混合物,沙子不溶于水,则选择过滤法分离,故选D;
②从碘水中提取碘单质,碘不易溶于水,易溶于有机溶剂,则利用有机溶剂萃取碘水中的碘,分液可分离,故选A;
③分离水和汽油的混合物,水和汽油分层,则选择分液法分离,故选F;
④分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物,CCl4和甲苯互溶,但沸点不同,则选择蒸馏法分离,故选E。

【题目】氯化亚铜(CuCl)常用作有机合成工业中的催化剂,在空气中迅速被氧化变成绿色;见光分解变成褐色。如图是工业上用制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl)生产CuCl的流程:
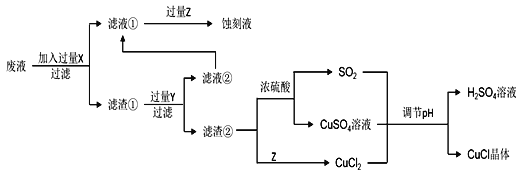
根据以上信息回答下列问题:
(1)生产过程中X的化学式为____。
(2)写出产生CuCl的离子方程式:____。
(3)实验探究pH对CuCl产率的影响如表所示:
pH | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
CuCl产率/% | 70 | 90 | 82 | 78 | 75 | 72 | 70 |
析出CuCl晶体最佳pH为____,当pH较大时CuCl产率变低原因是____。调节pH时,___(填“能”或“不能”)用相同pH的硝酸代替硫酸,理由是____。
(4)氯化亚铜的定量
①称取样品0.25g和过量的FeCl3溶液于锥形瓶中,充分溶解。
②用0.10mol·L1硫酸铈标准溶液滴定。已知:CuCl+FeCl3=CuCl2+FeCl2、Fe2++Ce4+=Fe3++Ce3+。三次平行实验结果如表(平行实验结果相差不能超过1%):
平行实验次数 | 1 | 2 | 3 |
0.25g样品消耗硫酸铈标准溶液的体积(mL) | 24.35 | 24.05 | 23.95 |
则样品中CuCl的纯度为_____。(结果保留三位有效数字)。
(5)由CuCl水解再热分解可得到纳米Cu2O。第一步CuCl水解的离子方程式为:CuCl(s)+H2O(l)![]() CuOH(s)+Cl (aq)+H+(aq),第二步CuOH热分解的化学方程式为____。第一步CuCl水解反应的平衡常数K与此温度下KW、Ksp(CuOH)、Ksp(CuCl)的关系为K=____。
CuOH(s)+Cl (aq)+H+(aq),第二步CuOH热分解的化学方程式为____。第一步CuCl水解反应的平衡常数K与此温度下KW、Ksp(CuOH)、Ksp(CuCl)的关系为K=____。