题目内容
【题目】一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如下图所示。下列判断不正确的是
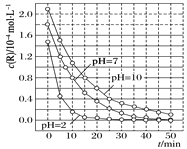
A. 溶液酸性越强,R的降解速率越大
B. 在0~50 min之间,pH=2和pH=7时R的降解百分率相等
C. 在20~25 min之间, pH=10时R的平均降解速率为4×10-6 mol·L-1·min-1
D. R的起始浓度越小,降解速率越大
【答案】D
【解析】pH分别为2、7、10时,通过曲线的倾斜和谐可看出溶液的酸性越强,R的降解速率越大,故A正确;由图知,在0-50min之间,pH=2和pH=7时反应物R都能完全反应,降解率都是100%,故B正确; 20-25min之间,pH=10时,R的平均降解速率为![]() mol/L。min,故C正确;R的起始浓度越大,降解速率越大,故D错误。
mol/L。min,故C正确;R的起始浓度越大,降解速率越大,故D错误。

练习册系列答案
相关题目

