题目内容
已知723 K时,2SO2(g)+O2(g)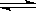 2SO3(g) ΔH=-Q,在相同条件下,向一密闭容器中通入2 mol SO2和1 mol O2,达到平衡时放出的热量为Q1;向另一体积相同的密闭容器中通入1 mol SO2和0.5 mol O2,达到平衡时放出的热量为Q2。则Q1、Q2、Q满足的关系是
2SO3(g) ΔH=-Q,在相同条件下,向一密闭容器中通入2 mol SO2和1 mol O2,达到平衡时放出的热量为Q1;向另一体积相同的密闭容器中通入1 mol SO2和0.5 mol O2,达到平衡时放出的热量为Q2。则Q1、Q2、Q满足的关系是
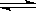 2SO3(g) ΔH=-Q,在相同条件下,向一密闭容器中通入2 mol SO2和1 mol O2,达到平衡时放出的热量为Q1;向另一体积相同的密闭容器中通入1 mol SO2和0.5 mol O2,达到平衡时放出的热量为Q2。则Q1、Q2、Q满足的关系是
2SO3(g) ΔH=-Q,在相同条件下,向一密闭容器中通入2 mol SO2和1 mol O2,达到平衡时放出的热量为Q1;向另一体积相同的密闭容器中通入1 mol SO2和0.5 mol O2,达到平衡时放出的热量为Q2。则Q1、Q2、Q满足的关系是| A.Q=2Q2 | B.Q1=2Q2 |
| C.Q=Q1>Q2 | D.Q>Q1>Q2 |
D
反应是可逆反应,所以2 mol SO2和1 mol O2不可能生成2mol三氧化硫,即放出的热量小于Q。如果SO2和氧气的浓度均减半,则相当于降低反应物浓度,平衡向逆反应方向移动,反应物的转化率降低,所以Q1>2Q2,因此答案选D。

练习册系列答案
相关题目
