题目内容
下列有关溶液中离子浓度的关系,不正确的是
- A.NaHCO3溶液中存在:c(OH-)=c(H2CO3)+c(H+)
- B.常温下,pH=3的盐酸和pH=ll的氨水等体积混合后,溶液中:c(NH4+)>c(Cl-)
- C.0.2 mol/LNH4Cl溶液与0.1 mol/L NaOH溶液等体积混合后,溶液中:c(NH4+)>c(Na+)
- D.0.2 mol/L 的 CH3COOH 溶液中c(H+)小于0.1 mol/L 的 CH3COOH 中c(H+)的两倍
A
试题分析:A、根据电荷守恒和物料守恒可知,c(HCO3-)+2c(CO32-)+c(OH-)=c(Na+)+c(H+)、c(HCO3-)+c(CO32-)+c(H2CO3)=c(Na+),所以c(CO32-)+c(OH-)=c(H2CO3)+c(H+),A不正确;B、氨水是弱碱,则pH=ll的氨水溶液的浓度大于0.001mol/L,则常温下,pH=3的盐酸和pH=ll的氨水等体积混合后,氨水过量,溶液显碱性。则根据电荷守恒可知c(NH4+)+c(H+)=c(Cl-)+c(OH-),所以溶液中c(NH4+)>c(Cl-),B正确;C、0.2 mol/LNH4Cl溶液与0.1 mol/L NaOH溶液等体积混合后生成一水合氨、氯化钠,氯化铵过量,且过量的氯化铵与生成的一水合氨的浓度相同。由于氨水的电离程度大于NH4+的水解程度,所以溶液中:c(NH4+)>c(Na+),C正确;D、醋酸是弱酸,存在电离平衡。稀释有利于电离,所以0.2 mol/L 的 CH3COOH 溶液的电离程度小于0.1 mol/L 的 CH3COOH溶液的电离程度,因此溶液中前者c(H+)小于后者c(H+)的两倍,D正确,答案选A。
考点:考查电离平衡、水解平衡以及溶液中离子浓度大小比较等
试题分析:A、根据电荷守恒和物料守恒可知,c(HCO3-)+2c(CO32-)+c(OH-)=c(Na+)+c(H+)、c(HCO3-)+c(CO32-)+c(H2CO3)=c(Na+),所以c(CO32-)+c(OH-)=c(H2CO3)+c(H+),A不正确;B、氨水是弱碱,则pH=ll的氨水溶液的浓度大于0.001mol/L,则常温下,pH=3的盐酸和pH=ll的氨水等体积混合后,氨水过量,溶液显碱性。则根据电荷守恒可知c(NH4+)+c(H+)=c(Cl-)+c(OH-),所以溶液中c(NH4+)>c(Cl-),B正确;C、0.2 mol/LNH4Cl溶液与0.1 mol/L NaOH溶液等体积混合后生成一水合氨、氯化钠,氯化铵过量,且过量的氯化铵与生成的一水合氨的浓度相同。由于氨水的电离程度大于NH4+的水解程度,所以溶液中:c(NH4+)>c(Na+),C正确;D、醋酸是弱酸,存在电离平衡。稀释有利于电离,所以0.2 mol/L 的 CH3COOH 溶液的电离程度小于0.1 mol/L 的 CH3COOH溶液的电离程度,因此溶液中前者c(H+)小于后者c(H+)的两倍,D正确,答案选A。
考点:考查电离平衡、水解平衡以及溶液中离子浓度大小比较等

练习册系列答案
相关题目
( 12 分)(1)某校化学兴趣小组用如下图所示过程除去AlCl3中含有的Mg2+、K+杂质离子并尽可能减少AlCl3的损失。请回答下列问题:
①写出混合物中加入足量氢氧化钠溶液时,溶液中发生反应的离子方程式:
。
②溶液a中存在的阴离子有__________________;在溶液a中加入盐酸时需控制溶液的pH的原因是_______________________________________;为此,改进方法是 。
?(2)?该化学小组又测定一定质量的某镁铝混合物中镁的质量分数,设计了如下实验方案:
方案Ⅰ:镁铝混合物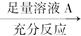 测定生成气体的体积
测定生成气体的体积
方案Ⅱ:镁铝混合物 测定剩余固体的质量
测定剩余固体的质量
下列有关判断中不正确的是 ?(填代号)
| A.溶液A选用NaOH溶液 |
| B.若溶液B选用浓硝酸,则测得镁的质量分数偏小 |
| C.溶液A和B均可选用稀硝酸 |
| D.实验室中方案Ⅱ更便于实施 |
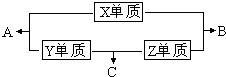 X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:
X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:





