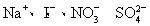题目内容
X、Y、Z是三种短周期的主族元素,在周期表中的位置如图所示,X原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( )
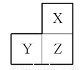
A.原子半径:Y>Z>X
B.气态氢化物的热稳定性:X<Z
C.Y和Z的最高价氧化物对应水化物均为强酸
D.若Z的最高正价为+m,则X的最高正价也一定为+m
A
【解析】因为X的最外层电子数是其次外层电子数的3倍,X为O,Z为S,Y为P。原子半径P>S>O,A对;H2O的热稳定性大于H2S的,B错;P的最高价含氧酸为H3PO4,S的最高价含氧酸为H2SO4,H3PO4为中强酸,C错;S的最高价为+6价,O无+6价,D错

 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案1 L 某混合溶液,可能含有的离子如下表:
可能大量含有的阳离子 | H+、K+、Mg2+、Al3+、 |
可能大量含有的阴离子 | Cl-、Br-、I-、 |
(1)往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示。则该溶液中一定不含有的离子是________________。

(2)BC段的离子方程式为__________________________。
(3)V1、V2与V3、V4之间的关系为____________________。
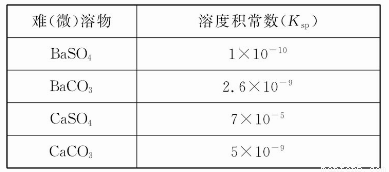
(4)经检测,该溶液中还含有大量的Cl-、Br-、I-,若向1 L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如表所示,分析后回答下列问题:
Cl2的体积(标准状况) | 2.8 L | 5.6 L | 11.2L |
n(Cl-) | 1.25 mol | 1.5 mol | 2 mol |
n(Br-) | 1.5 mol | 1.4 mol | 0.9 mol |
n(I-) | a mol | 0 | 0 |
①当通入Cl2的体积为2.8 L时,溶液中发生反应的离子方程式为____________________。
②原溶液中Cl-、Br-、I-的物质的量浓度之比为_________________。