题目内容
9.下列叙述正确的是( )| A. | 实验测定液态HCl、固体KNO3均不能导电,所以HCl、KNO3均是非电解质 | |
| B. | SO3溶于水能导电,但它是非电解质 | |
| C. | 有单质参加同时有单质生成的反应一定属于氧化还原反应 | |
| D. | 不与酸反应的氧化物一定会跟碱反应 |
分析 电解质:在水溶液中或熔融状态下能够导电的化合物;
非电解质:在熔融状态和水溶液中都不能导电的化合物.
解答 解:A.液态HCl、固态KNO3在水溶液中都能够导电,都是电解质,故A错误;
B.三氧化硫在水溶液中与水反应生成硫酸,硫酸电离出自由移动的离子导电,三氧化硫自身不能电离,是非电解质,故B正确;
C.氧气可以转化为臭氧,有单质参加和单质生成,但没有元素化合价的变化,不是氧化还原反应,故C错误;
D.CO不与酸反应,也不与碱反应,故D错误,
故选B.
点评 本题考查电解质、非电解质概念的辨析,难度不大.解题时紧抓住电解质必须是化合物,以及导电是在水溶液或熔化状态下为条件.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.某有机物M的结构简式为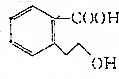 ,下列有关M的说法正确的是( )
,下列有关M的说法正确的是( )
 ,下列有关M的说法正确的是( )
,下列有关M的说法正确的是( )| A. | M的分子式为C9H10O3 | |
| B. | M 可使酸性KMnO4溶液褪色 | |
| C. | 1 mol M完全燃烧消耗10 mol O2 | |
| D. | 1 mol M能与足量Na反应生成0.5 mol H2 |
20.已知CO(g)+H2O(g)?CO2(g)+H2(g)反应的平衡常数和温度的关系如下:
回答下列问题:
(1)该反应的△H<0(填“<”“>”“=”);
(2)830℃时,向一个5L的密闭容器中充入0.20mol的CO和0.80mol的H2O,反应初始6s内CO的平均反应速率v(CO)=0.003mol•L-1•s-1,则6s末CO2的物质的量浓度为0.018mol/L;反应达到平衡后CO的转化率为80%;
(3)判断该反应是否达到平衡状态的依据为cd(填正确选项前的字母);
a.压强不随时间改变 b.气体的密度不随时间改变
c.c(CO)不随时间改变 d.单位时间里生成CO和H2的物质的量相等
(4)已知1000℃时,要使CO的转化率超过90%,则起始时c(H2O):c(CO)应不低于14.4;
(5)某燃料电池以CO为燃料,以空气为氧化剂,以熔融态的K2CO3为电解质,请写出该燃料电池正极的电极反应式O2+4e-+2CO2═2CO32-;
(6)已知CO可用于制备很多物质:
2CO(g)+SO2(g)═S(g)+2CO2(g)△H=+18.0kJ•mol-1
2H2(g)+SO2(g)═S(g)+2H2O(g)△H=+90.4kJ•mol-1
2CO(g)+O2(g)═2CO2(g)△H=-556.0kJ•mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1
请写出S(g)与O2(g)反应生成SO2(g)热化学方程式S(g)+O2(g)=SO2(g)△H=-574.0kJmol-1.
| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
(1)该反应的△H<0(填“<”“>”“=”);
(2)830℃时,向一个5L的密闭容器中充入0.20mol的CO和0.80mol的H2O,反应初始6s内CO的平均反应速率v(CO)=0.003mol•L-1•s-1,则6s末CO2的物质的量浓度为0.018mol/L;反应达到平衡后CO的转化率为80%;
(3)判断该反应是否达到平衡状态的依据为cd(填正确选项前的字母);
a.压强不随时间改变 b.气体的密度不随时间改变
c.c(CO)不随时间改变 d.单位时间里生成CO和H2的物质的量相等
(4)已知1000℃时,要使CO的转化率超过90%,则起始时c(H2O):c(CO)应不低于14.4;
(5)某燃料电池以CO为燃料,以空气为氧化剂,以熔融态的K2CO3为电解质,请写出该燃料电池正极的电极反应式O2+4e-+2CO2═2CO32-;
(6)已知CO可用于制备很多物质:
2CO(g)+SO2(g)═S(g)+2CO2(g)△H=+18.0kJ•mol-1
2H2(g)+SO2(g)═S(g)+2H2O(g)△H=+90.4kJ•mol-1
2CO(g)+O2(g)═2CO2(g)△H=-556.0kJ•mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1
请写出S(g)与O2(g)反应生成SO2(g)热化学方程式S(g)+O2(g)=SO2(g)△H=-574.0kJmol-1.
17.下列关于配合物的说法中,正确的是( )
| A. | 配合物的外界是指配合物中的阴离子 | |
| B. | 只有过渡金属元素能形成配合物 | |
| C. | Fe(SCN)3不属于配合物 | |
| D. | Na3[AlF6]的中心原子的配位数为6 |
4.在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是( )
| A. | 甲的分子数比乙的分子数多 | |
| B. | 甲的物质的量比乙的物质的量小 | |
| C. | 甲的气体摩尔体积比乙的气体摩尔体积小 | |
| D. | 甲的相对分子质量比乙的相对分子质量小 |
14.茶叶中铁元素检验可用以下步骤完成,各步骤选用实验用品不能都用到的( )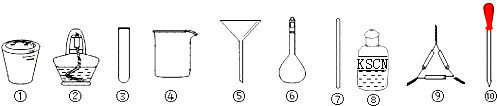

| A. | 将茶叶灼烧灰化,选用①、②和⑨ | |
| B. | 过滤得到滤液,选用④、⑤和⑦ | |
| C. | 用浓硝酸溶解茶叶灰并加蒸馏水稀释,选用④、⑥和⑦ | |
| D. | 检验滤液中的Fe3+,选用③、⑧和⑩ |
18.糖类是由C、H、O三种元素组成的一类有机化合物,糖类也叫碳水化合物,原因是它们的化学组成大多符合通式Cn(H2O)m.葡萄糖的分子式是C6H12O6,属于单糖(填“单糖”、“二糖”或“多糖”).
19.下列对人体健康无害的是( )
| A. | 用工业石蜡给瓜子美容 | B. | 用工业酒精(含甲醇)配兑饮用酒 | ||
| C. | 食用加碘盐预防碘缺乏病 | D. | 食用亚硝酸盐超标的腊肉 |
