题目内容
4.在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是( )| A. | 甲的分子数比乙的分子数多 | |
| B. | 甲的物质的量比乙的物质的量小 | |
| C. | 甲的气体摩尔体积比乙的气体摩尔体积小 | |
| D. | 甲的相对分子质量比乙的相对分子质量小 |
分析 由PV=nRT=$\frac{m}{M}$RT,可知PM=ρRT,可知同温同压下,气体密度之比等于其摩尔质量之比,同温同压下甲的密度大于乙的密度,则M(甲)>M(乙);
A.根据n=$\frac{m}{M}$判断二者物质的量大小,物质的量越大,含有分子数目越多;
B.根据n=$\frac{m}{M}$判断二者物质的量之比;
C.温度、压强相同,气体摩尔体积相同;
D.相对分子质量之比等于其摩尔质量之比.
解答 解:由PV=nRT=$\frac{m}{M}$RT,可知PM=ρRT,可知同温同压下,气体密度之比等于其摩尔质量之比,同温同压下甲的密度大于乙的密度,则M(甲)>M(乙).
A.由于M(甲)>M(乙),根据n=$\frac{m}{M}$可知,等质量甲、乙物质的量为n(甲)<n(乙),故乙含有分子数目较多,故A错误;
B.由于M(甲)>M(乙),根据n=$\frac{m}{M}$可知,等质量甲、乙物质的量为n(甲)<n(乙),故B正确;
C.温度、压强相同,气体摩尔体积相同,故C错误;
D.相对分子质量之比等于其摩尔质量之比,故Mr(甲)>Mr(乙),故D错误,
故选:B.
点评 本题考查阿伏伽德罗定律及其推论,注意根据PV=nRT理解阿伏伽德罗定律及其推论,难度不大.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目
14.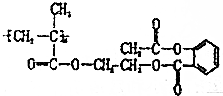 某药物的结构式如图所示,使其与含1.2g NaOH的溶液反应完全,消耗该药物的质量为( )
某药物的结构式如图所示,使其与含1.2g NaOH的溶液反应完全,消耗该药物的质量为( )
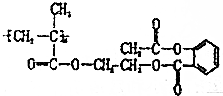 某药物的结构式如图所示,使其与含1.2g NaOH的溶液反应完全,消耗该药物的质量为( )
某药物的结构式如图所示,使其与含1.2g NaOH的溶液反应完全,消耗该药物的质量为( )| A. | 2.19n g | B. | 2.19g | C. | $\frac{2.92}{n}$g | D. | 2.92g |
19.等物质的量的下列化合物在相应条件下完全分解后,得到O2的质量最多的是( )
| A. | KClO3(加MnO2催化剂,加热) | B. | KMnO4(加热) | ||
| C. | H2O2(水溶液,加MnO2催化剂) | D. | HgO(加热) |
9.下列叙述正确的是( )
| A. | 实验测定液态HCl、固体KNO3均不能导电,所以HCl、KNO3均是非电解质 | |
| B. | SO3溶于水能导电,但它是非电解质 | |
| C. | 有单质参加同时有单质生成的反应一定属于氧化还原反应 | |
| D. | 不与酸反应的氧化物一定会跟碱反应 |
16.室温下,下列溶液中的微粒浓度关系正确的是( )
| A. | 由pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | CH3COONa溶液中:c(Na+)=c(CH3COO-)+c(OH-) | |
| C. | Na2CO3溶液:c(Na+)+c(H+)=2c(CO32-)+c(OH-) | |
| D. | (NH4)2SO4溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) |
13.能使发热的病人体温降至正常,并起到缓解疼痛的作用,该药物是( )
| A. | 阿司匹林(乙酰水杨酸) | B. | 青霉素 | ||
| C. | 抗酸药(氢氧化铝) | D. | 麻黄碱 |
14.下列操作或发生事故时的处理方法正确的是( )
| A. | 将pH试纸用蒸馏水润湿后,测定稀盐酸的pH值 | |
| B. | 给试管里的液体加热时,试管应与桌面垂直 | |
| C. | 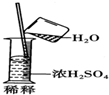 | |
| D. | 浓硫酸不慎沾在皮肤上,应立即用干布拭去,然后用水冲洗,最后再涂上3%~5%的小苏打溶液 |
 如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据
如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据