题目内容
4.某元素是公认的“智慧元素”,尤其是脑机能中起着十分重要的作用,儿童缺它会导致发育迟缓,成人缺它会引起甲状腺肿大.你认为该元素是( )| A. | 钙 | B. | 磷 | C. | 铁 | D. | 碘 |
分析 缺碘会引起甲状腺肿大,据此解题.
解答 解:A.缺钙可能导致幼儿及青少年发育不良,严重时还会患佝偻病,故A错误;
B.缺磷会引起骨骼,牙齿发育不正常,故B错误;
C.缺铁会导致缺铁性贫血,故C错误;
D.碘被公认为人类的“智慧元素”.儿童缺它会导致发育迟缓,成人缺它会引起甲状腺肿大,故D正确,
故选D.
点评 本题考查微量元素对人体的重要作用,难度不大,要注意平时知识的积累.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案
相关题目
15.下列物质分类正确的是( )
| A. | SO2、SiO2、CO均为酸性氧化物 | |
| B. | Cu、NaCl、CaO在熔融状态下均能导电 | |
| C. | 烧碱、硫酸、四氯化碳均为电解质 | |
| D. | 稀豆浆、牛奶、氯化铁溶液均为胶体 |
12.下列关于Na2O和Na2O2的叙述正确的是( )
| A. | Na2O与Na2O2颜色相同 | |
| B. | Na2O和Na2O2都是碱性氧化物 | |
| C. | Na2O与Na2O2都能用于漂白,杀菌、消毒 | |
| D. | 阴阳离子的个数比均为1:2 |
19. 下列两种方案制备氢氧化铝
下列两种方案制备氢氧化铝
Ⅰ:2.7gAl $\stackrel{100mL稀盐酸}{→}$X溶液 $\stackrel{NaOH溶液}{→}$氢氧化铝
Ⅱ2.7gAl $\stackrel{100mLNaOH溶液}{→}$Y溶液 $\stackrel{稀盐酸}{→}$氢氧化铝
已知所用的稀盐酸与NaOH溶液均为3mol/L.如图是向X溶液与Y溶液中分别加入NaOH溶液或稀盐酸时产生沉淀的质量与加入溶液体积之间的关系.相关说法正确的是( )
 下列两种方案制备氢氧化铝
下列两种方案制备氢氧化铝 Ⅰ:2.7gAl $\stackrel{100mL稀盐酸}{→}$X溶液 $\stackrel{NaOH溶液}{→}$氢氧化铝
Ⅱ2.7gAl $\stackrel{100mLNaOH溶液}{→}$Y溶液 $\stackrel{稀盐酸}{→}$氢氧化铝
已知所用的稀盐酸与NaOH溶液均为3mol/L.如图是向X溶液与Y溶液中分别加入NaOH溶液或稀盐酸时产生沉淀的质量与加入溶液体积之间的关系.相关说法正确的是( )
| A. | 方案二比方案一生成更多的气体 | |
| B. | a曲线表示的是向Y溶液中加入稀盐酸溶液 | |
| C. | 在M点时,两种方案中所得溶液的溶质质量分数相同 | |
| D. | M点以后,a、b两条曲线将重合为一条 |
16.与100mL 0.5mol/L氯化铝溶液中的氯离子物质的量浓度相等的溶液是( )
| A. | 50mL 1.5mol/L的KCl溶液 | B. | 50mL 1.5mol/L的KClO3溶液 | ||
| C. | 100mL 1mol/L的MgCl溶液 | D. | 450mL 0.5mol/的NaCl溶液 |
7.工业上用N2和H2 合成NH3“N2(g)+3H2(g)═2NH3(g)△H<0”,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:

(1)已知:N2(g)+O2(g)=2NO(g)△H=+a kJ•mol-1
N2(g)+3H2(g)═2NH3(g)△H=-b kJ•mol-1
2H2(g)+O2(g)=2H2O(g)△H=-c kJ•mol-1(a、b、c均为正值)
若有34g 氨气经催化氧化完全生成一氧化氮气体和水蒸气所放出的热量为$\frac{1}{2}$(2a-2b+3c)kJ.
(2)合成NH3达到平衡后,某时刻改变下列条件A,在达到新平衡的过程中正反应速率始终增大.
A.升温 B.加压 C.增大c(N2) D.降低c(NH3)
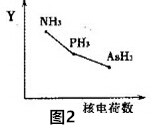
(3)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对合成NH3反应的影响.实验结果如图1所示:(图中T表示温度,n表示起始时H2物质的量)
①图象中T2和T1的关系是:T2<T1(填“>”、“<”、“=”或“无法确定”).
②比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最大的是c(填字母).
③若容器容积为1L,b点对应的n=0.15mol,测得平衡时H2的转化率为60%,则平衡时N2的物质的量浓度为0.05 mol•L-1.
(4)一定温度下,将2mol N2和4mol H2置于1L的恒容密闭容器中反应,测得不同条件、不同时间段内合成NH3反应中N2的转化率,得到数据如下表:
上表中a、b、80%三者的大小关系为80%<a=b或80%<a<b.(填“>”、“=”、“<”、“无法比较”)
(5)在图2中画出(4)中T1温度下2mol N2和4mol H2在1L容器中反应,3小时达平衡前后过程中N2和NH3的物质的量浓度随时间的变化曲线图.

(1)已知:N2(g)+O2(g)=2NO(g)△H=+a kJ•mol-1
N2(g)+3H2(g)═2NH3(g)△H=-b kJ•mol-1
2H2(g)+O2(g)=2H2O(g)△H=-c kJ•mol-1(a、b、c均为正值)
若有34g 氨气经催化氧化完全生成一氧化氮气体和水蒸气所放出的热量为$\frac{1}{2}$(2a-2b+3c)kJ.
(2)合成NH3达到平衡后,某时刻改变下列条件A,在达到新平衡的过程中正反应速率始终增大.
A.升温 B.加压 C.增大c(N2) D.降低c(NH3)
(3)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对合成NH3反应的影响.实验结果如图1所示:(图中T表示温度,n表示起始时H2物质的量)
①图象中T2和T1的关系是:T2<T1(填“>”、“<”、“=”或“无法确定”).
②比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最大的是c(填字母).
③若容器容积为1L,b点对应的n=0.15mol,测得平衡时H2的转化率为60%,则平衡时N2的物质的量浓度为0.05 mol•L-1.
(4)一定温度下,将2mol N2和4mol H2置于1L的恒容密闭容器中反应,测得不同条件、不同时间段内合成NH3反应中N2的转化率,得到数据如下表:
| 时间 N2的转化率 温度 | 1小时 | 2小时 | 3小时 | 4小时 |
| T1 | 30% | 50% | 80% | 80% |
| T2 | 35% | 60% | a | b |
(5)在图2中画出(4)中T1温度下2mol N2和4mol H2在1L容器中反应,3小时达平衡前后过程中N2和NH3的物质的量浓度随时间的变化曲线图.
8.下列叙述正确的是( )
| A. | 若0.1mol•L-1的醋酸溶液pH=a,将其稀释10倍后,溶液的pH=b,则a+1>b | |
| B. | 在滴有酚酞溶液的氨水里,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7 | |
| C. | 1.0×10-3mol/L盐酸的pH=3,1.0×10-8mol/L盐酸的pH=8 | |
| D. | 某温度下,若1mL pH=1的盐酸与100mL NaOH溶液混合后,溶液的pH=7;则NaOH溶液的pH=11 |

 .
. .
. .
.