题目内容
【题目】在一密闭容器中发生下列反应:N2(g)+3H2(g) ![]() 2NH3(g)(正反应为放热反应),下图是某一时间段反应速率与反应进程的关系曲线图。
2NH3(g)(正反应为放热反应),下图是某一时间段反应速率与反应进程的关系曲线图。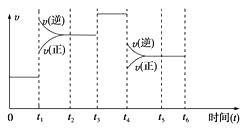
(1)t1、t3、t4时刻,体系中分别是什么条件发生了变化?
t1 , t3 , t4。
(2)下列时间段中,氨的百分含量最高的是( )
A.0~t1 B.t2~t3
C.t3~t4 D.t4~t5
【答案】
(1)升温,加入催化剂,减压
(2)A
【解析】在t1时刻,正、逆反应速率都增大,且逆反应速率大于正反应速率,则平衡逆向移动,满足两个要求的条件为升温;在t3时刻,正、逆反应速率同等程度增大,则条件为加入催化剂;在t4时刻,正、逆反应速率都减小,且逆反应速率大于正反应速率,则平衡逆向移动,满足两个要求的条件为减压。改变三种条件,一种不影响氨的百分含量,两种都使平衡向逆反应方向移动,氨的百分含量减小,所以在0~t1时间段,氨的百分含量最大。
根据正逆反应速率的变化判断化学平衡移动的方向和改变的外界条件即可.

练习册系列答案
相关题目