题目内容
【题目】写出下对反应的化学方程式,并注明反应类型:
(1)乙醇制乙烯:__,反应类型:__。
(2)乙醇与浓氢溴酸反应:__,反应类型__。
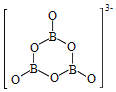
(3)苯酚与浓溴水反应:__,反应类型__。
(4)乙醛与新制氢氧化铜悬浊液反应:__,反应类型__。
【答案】CH3—CH2OH![]() CH2=CH2↑+H2O 消去反应 CH3CH2OH+HBr
CH2=CH2↑+H2O 消去反应 CH3CH2OH+HBr![]() CH3—CH2—Br+H2O 取代反应
CH3—CH2—Br+H2O 取代反应 ![]() +3Br2
+3Br2 ↓+3HBr 取代反应 CH3CHO+NaOH+2Cu(OH)2
↓+3HBr 取代反应 CH3CHO+NaOH+2Cu(OH)2![]() CH3COONa+Cu2O↓+3H2O 氧化反应
CH3COONa+Cu2O↓+3H2O 氧化反应
【解析】
(1)乙醇和浓硫酸混合加热至170℃,发生消去反应得到乙烯:CH3—CH2OH![]() CH2=CH2↑+H2O。
CH2=CH2↑+H2O。
(2)乙醇与浓氢溴酸共热,发生取代反应,生成溴乙烷和水:CH3CH2OH+HBr![]() CH3—CH2—Br+H2O。
CH3—CH2—Br+H2O。
(3)苯酚与浓溴水混合,发生取代反应,苯环上和连接羟基的碳原子处于邻对位的碳原子上的氢原子被溴原子取代,生成三溴苯酚白色沉淀:![]() +3Br2
+3Br2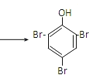 ↓+3HBr。
↓+3HBr。
(4)乙醛与新制氢氧化铜悬浊液共热,乙醛被氧化,在碱性溶液中生成乙酸盐,同时生成红色沉淀氧化亚铜:CH3CHO+NaOH+2Cu(OH)2![]() CH3COONa+Cu2O↓+3H2O。
CH3COONa+Cu2O↓+3H2O。

 名校课堂系列答案
名校课堂系列答案【题目】已知:①(![]() +HNO3
+HNO3![]()
![]() +H2O △H<0;②硝基苯沸点210.9℃,蒸馏时选用空气冷凝管。下列制取硝基苯的操作或装置(部分夹持仪器略去),正确的是
+H2O △H<0;②硝基苯沸点210.9℃,蒸馏时选用空气冷凝管。下列制取硝基苯的操作或装置(部分夹持仪器略去),正确的是
选项 | A | B | C | D |
装置 |
|
|
|
|
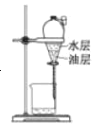
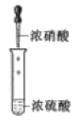
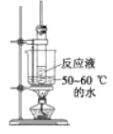
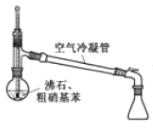
目的 | 分液 | 配制混酸 | 水浴加热 | 蒸馏提纯 |
A.AB.BC.CD.D
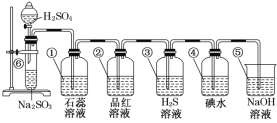
【题目】某兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”实验,以确保化学实验的绿色化。
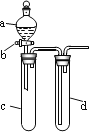
(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c。其目的是_____________________________________________________________________。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL的浓硝酸。反应一段时间后,再由a向c中加2 mL蒸馏水,c中的实验现象有什么变化___________。
方案 | 甲 | 乙 | 丙 |
反应物 | Cu、浓HNO3 | Cu、稀HNO3 | Cu、O2、稀HNO3 |
(3)如表所示是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是__________,理由是________________________________________________________________________。