题目内容
【题目】10.6g Na2CO3固体溶于水,配制成1L溶液,计算浓度是多少?
【答案】0.1mol/L
【解析】
10.6g Na2CO3固体的物质的量是10.6g÷106g/mol=0.1mol,溶于水,配制成1L溶液,因此碳酸钠的浓度是0.1mol÷1L=0.1mol/L。

练习册系列答案
相关题目
【题目】某无色稀溶液X中,可能含有下表所列离子中的某几种。
阴离子 | CO |
阳离子 | Al3+、Fe3+、Mg2+、NH |
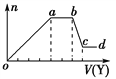
现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(V)的关系如图所示。
(1)若Y是盐酸,则oa段转化为沉淀的离子(指来源于X溶液的,下同)是________, bc段发生反应的离子方程式是________________________,
(2)若Y是NaOH溶液,则X中一定含有的离子是______________________,bc段发生反应的离子方程式是_____________________________________。