题目内容
【题目】氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是( )
A.加入少量水,水的电离平衡向电离方向移动
B.再通入少量氯气,Cl2+H2O![]() HCl+HCIO,平衡向正方向移动,c(Cl2)减少
HCl+HCIO,平衡向正方向移动,c(Cl2)减少
C.通入少量SO2,溶液漂白性增强
D.加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-)
【答案】A
【解析】
A.氯气和水反应生成盐酸和次氯酸,抑制水的电离,加入少量水,溶液中的氢离子浓度减小,水电离平衡正向移动,故正确;
B.通入少量氯气,平衡正向移动,但氯气的浓度增大,故错误;
C.通入少量二氧化硫,氯气和二氧化硫反应生成硫酸和盐酸,溶液的次氯酸减少,漂白性减弱,故错误;
D.加入少量固体氢氧化钠,反应生成氯化钠和次氯酸钠,根据电荷守恒有c(Na+)+ c(H+)=c(Cl-)+c(ClO-),故错误。
故选A。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
【题目】X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
元素 | 相关信息 |
X | X的价电子排布式为nsnnpn |
Y | Y的负一价离子的电子层结构都与氩相同 |
Z | 常温常压下,Z单质是淡黄色固体,常在火山口附近沉积 |
W | W原子共有6个价电子,其中五个价电子位于第三能层d轨道 |
(1)Z在元素周期表中的位置 _______________________,Z的氢化物空间构型是________
(2)在H—Y、H—Z两种共价键中,键的极性较强的是____________(用相应的元素符号表示该共价键)。
(3)XZ2分子中X以________方式杂化。
(4)写出W元素的原子核外电子排布式___________________________________。
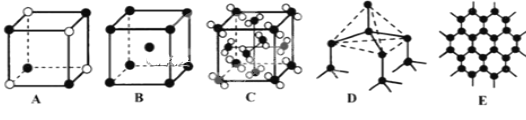
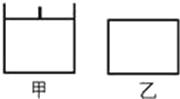
(5)Y元素和Na形成晶体的部分结构可用下图中的_________来表示(填序号)。