题目内容
【题目】燃煤脱硫可减少SO2的排放,燃煤脱硫技术受到各界科研人员的关注。某种燃煤脱硫技术的原理为CaO(s)+3CO(g)+SO2(g) CaS(s)+3CO2(g) ΔH=-394.0 kJ·mol-1。保持其他条件不变,平衡时CO2的体积分数随起始CO物质的量的变化关系如图所示:
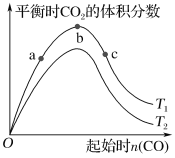
下列有关说法正确的是( )
A.T1>T2
B.T1时,b点对应状态的SO2转化率最高
C.T1时,b点后曲线下降是因为CO质量分数升高
D.减小压强可提高CO、SO2转化率
【答案】C
【解析】
A. CaO(s)+3CO(g)+SO2(g) CaS(s)+3CO2(g) ΔH=-394.0 kJ·mol-1,正反应是放热反应,升高温度,平衡逆向移动,二氧化碳的含量减少,所以由图可知T1<T2,A项错误;
B. 增加一种反应物的用量,可以提高另一种反应物的转化率,而本身的转化率降低,则CO的用量越多,二氧化硫的转化率越大,所以a点二氧化硫的转化率最低,而c点二氧化硫的转化率最高,B项错误;
C. 一氧化碳的物质的量增加,导致一氧化碳体积分数变大,二氧化碳的体积分数减小,所以b点后曲线下降是因为CO质量分数升高,C项正确;
D. CaO(s)+3CO(g)+SO2(g) CaS(s)+3CO2(g),正反应是气体体积减小的反应,所以减小压强,平衡逆向移动,则CO、SO2的转化率降低,D项错误;
答案选C。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】煤化工中常需研究不同温度下平衡常数、投料比及热值等问题。已知:CO(g)+H2O(g)H2(g)+CO2(g)平衡常数随温度的变化如下表:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
试回答下列问题:
(1)上述正向反应是________反应 (填“放热”或“吸热”);
(2)下列条件的改变能加快其反应速率的是_______(选填序号);
①升高温度;②保持体积不变,只增加CO的质量;③保持体积不变,充入Ne使体系压强增大;④保持压强不变,充入Ne使容器的体积增大
(3)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2,发生反应CO(g)+2H2(g) CH3OH(g),CO的平衡转化率与温度,压强的关系如下图所示:
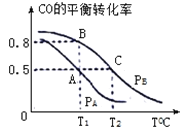
①A、B两点对应的压强大小关系是PA________PB;(填“>”,“<”,“=”)
②A、B、C三点的平衡常数KA、KB、KC的大小关系是 ____________;
③在P1压强、T1℃时,该反应的平衡常数K=___________;
(4)T1℃、1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下:CO:0.1mol H2:0.2mol CH3OH:0.2mol。此时v正 ____ v逆(填 >、< 或 =)。