题目内容
在2L的密闭容器中,充入1molSO2和1molO2,在一定条件下发生反应:2SO2+O2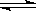 2SO3,当反应进行了10s时,测得SO2的物质的量为0.6mol,求:
2SO3,当反应进行了10s时,测得SO2的物质的量为0.6mol,求:
(1)用SO2表示该化学反应速率为多少?
(2)若改用O2表示化学反应速率又为多少?
(3)若要提高反应速率你认为可采取的合理措施有哪些?
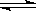 2SO3,当反应进行了10s时,测得SO2的物质的量为0.6mol,求:
2SO3,当反应进行了10s时,测得SO2的物质的量为0.6mol,求:(1)用SO2表示该化学反应速率为多少?
(2)若改用O2表示化学反应速率又为多少?
(3)若要提高反应速率你认为可采取的合理措施有哪些?
(1)0.02mol.L-1.S-1(2)0.01mol.L-1.S-1
(3)略
(3)略
试题分析: 2SO2 + O2
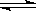 2SO3
2SO3起始浓度(mol/L) 0.5 0.5 0
转化浓度(mol/L) 0.2 0.1 0.2
10s时浓度(mol/L) 0.3 0.4 0.2
所以用SO2表示该化学反应速率为0.2mol/L÷10s=0.02mol/(L·s)
用O2表示化学反应速率0.1mol/L÷10s=0.02mol/(L·s)
在其它条件不变的情况下,可以通过增大压强或升高温度或会增大反应物的浓度使用催化剂等加快反应速率
点评:该题是基础性试题的考查,侧重对学生基础知识巩固和训练的同时,有利于培养考查学生灵活运用基础知识解决实际问题的能力,也有助于培养学生的逻辑推理和规范答题能力,提高学生的答题效率。

练习册系列答案
相关题目
 ,n=
,n= CH3OH(g),6秒末时容器内压强为开始时的0.6倍。试计算:(写出计算过程)
CH3OH(g),6秒末时容器内压强为开始时的0.6倍。试计算:(写出计算过程) 2C+D来说,下列反应速率最快的是 ( )
2C+D来说,下列反应速率最快的是 ( ) 2AB3的反应,以下反应速率的表示中,速率最快的是( )
2AB3的反应,以下反应速率的表示中,速率最快的是( )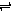 2C(g)若经 2 s(秒)后测得 C 的浓度为 0.6 mol?L-1,
2C(g)若经 2 s(秒)后测得 C 的浓度为 0.6 mol?L-1,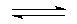 cC(g),此反应是放热反应。关于化学反应速率的叙述正确的是 ( )
cC(g),此反应是放热反应。关于化学反应速率的叙述正确的是 ( ) 2NH3(g)。经过5s后,测得N2剩余2.0 mol,在这5S内N2的反应速率为
2NH3(g)。经过5s后,测得N2剩余2.0 mol,在这5S内N2的反应速率为 L-1
L-1