题目内容
(10分)现有部分短周期元素的性质或原子结构如下表:
|
元素编号 |
元素性质或原子结构 |
|
T |
M层上有2对成对电子 |
|
X |
基态原子核外电子共占据5个原子轨道且有2个未成对电子, |
|
Y |
常温下单质为双原子分子,其氢化物水溶液呈碱性 |
|
Z |
元素最高正价是+7价 |
(1)元素T的原子最外层共有________种不同运动状态的电子。
(2) 元素Z与元素T相比,非金属性较强的是________(用元素符号表示),
(3)下列表述中能证明“元素Z与元素T相比,非金属性较强的”这一事实的是________。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)元素X和元素Y的第一电离能的大小关系为_________,请说明理由_______________。
(5)CO和Y2是等电子体,CO和Y2的结构均可表示为A≡B的形式(A、B可表示相同元素的原子也可表示不同元素的原子)。下表是两者的键能数据:(单位:kJ/mol)
|
|
A-B |
A=B |
A≡B |
|
CO |
357.7 |
798.9 |
1071.9 |
|
Y2 |
154.8 |
418.4 |
941.7 |
结合数据说明CO比Y2活泼的原因:______________________________________。
【答案】
(1)6(2分) (2) Cl(1分) (3) b(1分)
(4)N>O(1分) N原子的外围电子排布式为2s2sp3,2p轨道处于半充满状态,处于能量较低的稳定状态。(2分)
(5)断裂CO中第一个π键的键能是273kJ/mol,断裂N2中第一个π键的键能是523.3kJ/mol,所以CO的第一个键比N2更容易断。(3分)
【解析】略

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
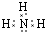
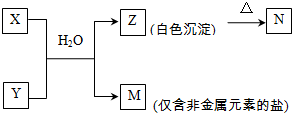
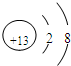
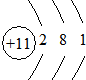
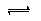 Al(OH)3
Al(OH)3 Al3++3OH-
Al3++3OH-