题目内容
【题目】研究化学反应的快慢和限度具有十分重要的意义。
回答下列问题:
(1)反应2SO2(g) + O2(g)![]() 2SO3(g)是制备硫酸的重要反应,该反应为放热反应。降低温度,逆反应的速率_________;使用催化剂V2O5,正反应的速率__________ (以上填“增加”、“不变”或“减小”), 催化剂对该反应的平衡状态_________影响(“有”或“无”)。
2SO3(g)是制备硫酸的重要反应,该反应为放热反应。降低温度,逆反应的速率_________;使用催化剂V2O5,正反应的速率__________ (以上填“增加”、“不变”或“减小”), 催化剂对该反应的平衡状态_________影响(“有”或“无”)。
(2)常温下,实验室用100 mL 6.0 mol·L-1硫酸跟足量锌粉反应制取氢气。
①为降低反应进行的速率,又不影响生成氢气的量,可向反应物中加入____(填序号 )。
A.CH3COONa固体 B.KNO3固体
C.K2SO4溶液 D.KHSO4溶液
②向溶液中滴加少量硫酸铜溶液,反应速率加快,原因是___________________。
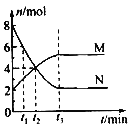
(3)一定温度下,在体积固定的密闭容器中,有色气体N与无色气体M的物质的量随时间变化曲线如图所示。图中能够表明起始加入的物质是__________________,反应达平衡的时间是____________,该反应的化学方程式可表示为______________________________;下列说法中能够判定该反应处于平衡状态的是______________填 序号)。
A.容器的压强不再变化
B.气体的颜色不再变化
C.每反应2 mol的N生成1 mol的M
D.气体的密度不再发生变化
【答案】 减小 增加 无 AC 锌与硫酸铜反应置换出的铜,铜、锌和稀硫酸三者形成原电池,反应加快 M和N t3 2N![]() M AB
M AB
【解析】(1)降低温度,正反应和逆反应速率均减小;使用催化剂,降低了反应所需的活化能,提高了反应速率,故正反应速率增大,使用催化剂对化学平衡没有影响;正确答案:减小 ;增加 ;无。
(2)①硫酸为强酸,与CH3COONa反应生成弱酸醋酸,酸由强变弱,反应速率降低,但酸的总量不变,不影响生成氢气的量,A正确;KNO3固体溶解后完全电离产生NO3-,在酸性环境下具有强氧化性,与锌粉发生氧化还原反应产生NO,使生成氢气的量减少,B错误;加入 K2SO4溶液相当于稀释了反应物硫酸的浓度,反应速率降低,但是H+的物质的量不变,不影响生成氢气的量,C正确;KHSO4溶液完全电离产生H+,使溶液中的H+的物质的量增大,使生成氢气的量增大,D错误;综上所述,正确答案AC。
②锌与硫酸铜反应置换出的铜,铜、锌和稀硫酸三者形成原电池,反应速率加快;正确答案:锌与硫酸铜反应置换出的铜,铜、锌和稀硫酸三者形成原电池,反应速率加快。
(3 反应达到平衡时,反应物与生成物的物质的量均保持不变,故在t3时刻反应达到平衡;由图知,反应物为N,生成物为M,反应达到平衡时,二者消耗的物质的量之比为n(N):n(M)=(8-2):(5-2)=2:1,故该反应的化学方程式可表示为2N(g) ![]() M(g);该反应为非等体积反应,混合气体的总物质的量不变,压强也不再变化,反应达到平衡状态,A正确;N为有色气体、M为无色气体,当气体的颜色不再变化时,反应物N的物质的量不再变化,此时反应处于平衡状态,B正确。每反应2mol的N生成1mol的M只描述了正反应方向,不能判定该反应处于平衡状态,C错误;该反应中反应物与生成物均为气体,不论反应是否达到平衡状态,混合气体的质量均保持不变,且该反应在容积固定的密闭容器中进行,由
M(g);该反应为非等体积反应,混合气体的总物质的量不变,压强也不再变化,反应达到平衡状态,A正确;N为有色气体、M为无色气体,当气体的颜色不再变化时,反应物N的物质的量不再变化,此时反应处于平衡状态,B正确。每反应2mol的N生成1mol的M只描述了正反应方向,不能判定该反应处于平衡状态,C错误;该反应中反应物与生成物均为气体,不论反应是否达到平衡状态,混合气体的质量均保持不变,且该反应在容积固定的密闭容器中进行,由![]() 知,在整个反应过程中,气体的密度不发生变化,D错误;正确选项AB;正确答案:M和N;t3 ;2N
知,在整个反应过程中,气体的密度不发生变化,D错误;正确选项AB;正确答案:M和N;t3 ;2N![]() M ; AB。
M ; AB。