题目内容
【题目】(1)已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键需要的能量分别是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为_________________。
(2)已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,回答下列问题:
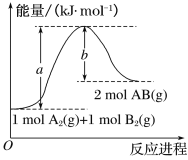
①该反应的ΔH_______0(填 “大于”“小于”或“等于”);
②反应物的总键能为______________;
③写出该反应的热化学方程式________________________________。
(3)联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) ΔH 4=-1048.9kJ/mol
写出联氨的结构式_______________,上述反应热效应之间的关系式为ΔH4=__________,联氨和N2O4可作为火箭推进剂的主要原因为_______________________________。
【答案】N2(g)+3H2(g)===2NH3(g) ΔH=-92 kJ·mol-1大于akJ·mol-1A2(g)+B2(g)===2AB(g) ΔH=+(a-b)kJ·mol-1![]() 2ΔH3-2ΔH2-ΔH1反应放热量大、产生大量气体、无污染
2ΔH3-2ΔH2-ΔH1反应放热量大、产生大量气体、无污染
【解析】
(1)根据“ΔH=反应物的键能总和-生成物的键能总和”计算。
(2)根据“反应物的总能量小于生成物的总能量”判断反应为吸热反应。结合图像书写热化学方程式。
(3)根据价键规则书写N2H4的结构式;根据盖斯定律分析反应热之间的关系。
(1)N2与H2反应生成NH3的化学方程式为N2(g)+3H2(g)=2NH3(g),该反应的ΔH=反应物的键能总和-生成物的键能总和=E(N≡N)+3E(H—H)-6E(N—H)=946kJ/mol+3×436kJ/mol-6×391kJ/mol=-92kJ/mol;N2与H2反应生成NH3的热化学方程式为:N2(g)+3H2(g)=2NH3(g) ΔH=-92kJ/mol。
(2)①1molA2(g)和1molB2(g)具有的总能量小于2molAB(g)具有的总能量,反应A2(g)+B2(g)=2AB(g)为吸热反应,ΔH大于0。
②根据图像,反应物的总键能为akJ/mol。
③根据图像,该反应的ΔH=+(a-b)kJ/mol,该反应的热化学方程式为:A2(g)+B2(g)=2AB(g) ΔH=+(a-b)kJ/mol。
(3)N原子最外层有5个电子,H原子最外层有1个电子,根据价键规则,N2H4的电子式为![]() ,N2H4的结构式为
,N2H4的结构式为![]() 。应用盖斯定律,消去O2(g)、H2(g),将③×2-①-②×2得④,则ΔH4=2ΔH3-ΔH1-2ΔH2。根据反应④知,联氨和N2O4可作为火箭推进剂的主要原因为:反应放热量大、产生大量气体、无污染。
。应用盖斯定律,消去O2(g)、H2(g),将③×2-①-②×2得④,则ΔH4=2ΔH3-ΔH1-2ΔH2。根据反应④知,联氨和N2O4可作为火箭推进剂的主要原因为:反应放热量大、产生大量气体、无污染。

 阅读快车系列答案
阅读快车系列答案


