题目内容
【题目】磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。
(1)基态O原子核外电子排布式为_______,基态Fe2+核外未成对电子数为_______,基态P原子核外占据最高能级的电子云轮廓图为_________形;
(2)比较大小(填“大于”、“小于”或“等于”):
①沸点:NH3_____PH3 ;②第一电离能:I1(P)_____I1(O)。
(3)PO43的空间构型是______,P原子的杂化形式为______,在1molPO43中含σ键______个。
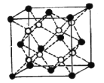
(4)Li2O的晶胞如图所示(其中白球代表Li,黑球代表O)。已知晶胞参数为0.4665 nm,阿伏加德罗常数的值为NA,则Li2O的密度为______g·cm3(列出计算式即可)。
【答案】1s22s22p4 4 纺锤 大于 小于 正四面体 sp3 4NA ![]()
【解析】
(1)根据电子排布规律书写;
(2)借助硫元素的位置,根据第一电离能的变化规律判断。
(3)根据价层电子互斥理论分析离子的空间构型和原子的杂化方式。
(4)根据晶胞的均摊法分析计算晶体的密度。
(1)基态氧原子的电子排布式为 1s22s22p4;基态Fe2+核外电子排布式为1s22s22p63s23p63d6,其中未成对电子数为4;基态P原子核外占据最高能级的电子为3p电子,其电子云轮廓图为纺锤形;
(2) ①氮的非金属性比磷强,所以氨气的稳定性大于磷化氢;
②同主族元素,从上往下第一电离能减小,同周期元素,从做到右,第一电离能增大,所以磷的第一电离能小于硫,硫小于氧。故I1(P) 小于I1(O);
(3)磷酸根离子中磷原子价层电子对个数为![]() ,且不含孤对电子,根据价层电子对互斥理论判断该阴离子为正四面体;中心原子磷原子杂化形式为 sp3;磷氧单键为σ键,磷氧双键为σ键和π键,所以一个磷酸根离子含有4个σ键,故1mol磷酸根离子含有 4NAσ 键。
,且不含孤对电子,根据价层电子对互斥理论判断该阴离子为正四面体;中心原子磷原子杂化形式为 sp3;磷氧单键为σ键,磷氧双键为σ键和π键,所以一个磷酸根离子含有4个σ键,故1mol磷酸根离子含有 4NAσ 键。
(4)由图可知,锂位于晶胞内部,氧位于顶点和面心,因此一个晶胞中有8个锂原子,氧原子个数为![]() =4,因此一个氧化锂晶胞的质量为
=4,因此一个氧化锂晶胞的质量为![]() g,一个晶胞的体积为(0.4665
g,一个晶胞的体积为(0.4665![]() )3cm3,即晶体的密度为
)3cm3,即晶体的密度为![]() g·cm3。
g·cm3。

 目标测试系列答案
目标测试系列答案【题目】温度为T时,向2.0L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g)![]() PCl3(g)+Cl2(g) 经一段时间后达到平衡。反应过程中测定的部分数据见下表:
PCl3(g)+Cl2(g) 经一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
下列说法正确的是
A.反应在前50 s的平均速率为v (PCl3) = 0.0032 mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时,c(PCl3) = 0.11 mol·L-1,则反应的ΔH < 0
C.相同温度下,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2,达到平衡前v (正) < v (逆)
D.相同温度下,起始时向容器中充入2.0 mol PCl5,达到平衡时PCl5的转化率小于20%