题目内容
【题目】人们常用催化剂来选择反应进行的方向.如图所示为一定条件下1mol CH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去].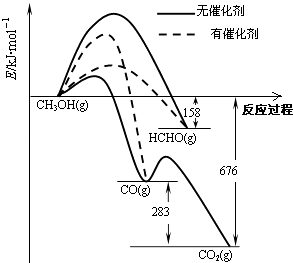
(1)①在有催化剂作用下,CH3OH与O2反应主要生成(填“CO、CO2”或“HCHO”).2HCHO(g)+O2(g)═2CO(g)+2H2O(g)△H= .
②甲醇制取甲醛可用Ag作催化剂,含有AgCl会影响Ag催化剂的活性.用氨水可以溶解除去其中的AgCl,写出该反应的离子方程式: .
(2)已知:CO(g)+2H2(g)CH3OH(g)△H=﹣a kJmol﹣1 .
①经测定不同温度下该反应的平衡常数如下:
温度(℃) | 250 | 300 | 350 |
K | 2.041 | 0.270 | 0.012 |
若某时刻、250℃测得该反应的反应物与生成物的浓度为c(CO)=0.4molL﹣1、c(H2)=0.4molL﹣1、c(CH3OH)=0.8molL﹣1 , 则此时v正v逆(填“>”、“<”或“=”).
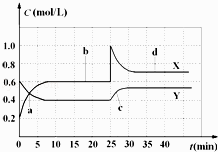
②某温度下,在体积固定的2L的密闭容器中将1mol CO和2mol H2混合,测得不同时刻的反应前后压强关系如下:
时间(min) | 5 | 10 | 15 | 20 | 25 | 30 |
压强比(P后/P前) | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
则0~15min,用H2表示的平均反应速率为 , 达到平衡时CO的转化率为 .
(3)利用钠碱循环法可除去SO2 , 消除SO2对环境的污染.吸收液吸收SO2的过程中,pH随n(SO32﹣):n(HSO3﹣)变化关系如下表:
n(SO32﹣):n(HSO3﹣) | 91:9 | 1:1 | 1:91 |
pH | 8.2 | 7.2 | 6.2 |
①根据上表判断NaHSO3溶液显性.
②在NaHSO3溶液中离子浓度关系正确的是 (填字母).
a.c(Na+)=2c(SO32﹣)+c(HSO3﹣)
b.c(Na+)>c(HSO3﹣)>c(H+)>c(SO32﹣)>c(OH﹣)
c.c(H2SO3)+c(H+)=c(SO32﹣)+(OH﹣)
d.c(Na+)+c(H+)=c(SO32﹣)+c(HSO3﹣)+c(OH﹣)
【答案】
(1)HCHO,﹣470kJ?mol﹣1,AgCl+2NH3?H2O=Ag(NH3)2++Cl﹣+2H2O或AgCl+2NH3=Ag(NH3)2++Cl﹣
(2)<,0.02mol?(L?min)﹣1,30%
(3)酸,bc
【解析】解:(1)①根据图象可以看出转化成甲醛时活化能最低,使用催化剂时主要产物为HCHO;
2HCHO(g)+O2(g)═2CO(g)+2H2O(g)该反应为放热反应,△H=﹣2(676﹣158﹣283)=﹣470KJmol﹣1,
所以答案是:HCHO;﹣470KJmol﹣1;
②氯化银与氨水发生络合反应的离子方程式:AgCl+2NH3H2O=Ag(NH3)2++Cl﹣+2H2O或者AgCl+2NH3=Ag(NH3)2++Cl﹣,
所以答案是:AgCl+2NH3H2O=Ag(NH3)2++Cl﹣+2H2O或AgCl+2NH3=Ag(NH3)2++Cl﹣;(2)①浓度商= ![]() =12.5>2.041,则平衡向逆反应方向移动,所以反应速率v正<v逆,所以答案是:<;
=12.5>2.041,则平衡向逆反应方向移动,所以反应速率v正<v逆,所以答案是:<;
②温度、体积不变的可逆反应中,气体的压强之比等于其物质的量之比,15min,压强比(P后/P前)=0.80,则反应后气体的物质的量=3mol×0.80=2.40mol,气体减少的物质的量=3mol﹣2.4mol=0.6mol,根据气体减少的物质的量与氢气之间的关系式知,参加反应的氢气的物质的量= ![]() =0.6mol,则氢气的反应速率=
=0.6mol,则氢气的反应速率= ![]() =0.02 mol( Lmin)﹣1;
=0.02 mol( Lmin)﹣1;
参加反应的CO的物质的量= ![]() =0.3mol,则CO的转化率=
=0.3mol,则CO的转化率= ![]() =30%,
=30%,
所以答案是:0.02 mol( Lmin)﹣1;30%;(3)①由表格中的数据可知,HSO3﹣越多,酸性越强,则电离生成氢离子,电离方程式为HSO3﹣H++SO32﹣,显酸性是因其电离大于其水解,
所以答案是:酸;
②a.根据物料守恒得c(Na+)=c(SO32﹣)+c(HSO3﹣)+c(H2SO3),亚硫酸氢根离子电离程度大于水解程度,所以c(SO32﹣)>c(H2SO3),所以c(Na+)<2c(SO32﹣)+c(HSO3﹣),故a错误;
b.亚硫酸氢根离子电离程度大于水解程度,溶液呈酸性,但电离和水解程度都较小,水还电离出氢离子,所以该溶液中离子浓度大小顺序是c(Na+)>c(HSO3﹣)>c(H+)>c(SO32﹣)>c(OH﹣),故b正确;
c.溶液中存在电荷守恒c(Na+)+c(H+)=2c(SO32﹣)+c(HSO3﹣)+c(OH﹣),物料守恒c(Na+)=c(SO32﹣)+c(HSO3﹣)+c(H2SO3),所以得c(H2SO3)+c(H+)=c(SO32﹣)+(OH﹣),故c正确;
d.根据电荷守恒得c(Na+)+c(H+)=2c(SO32﹣)+c(HSO3﹣)+c(OH﹣),故d错误;
故选bc.
【考点精析】本题主要考查了反应热和焓变和化学平衡状态本质及特征的相关知识点,需要掌握在化学反应中放出或吸收的热量,通常叫反应热;化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)才能正确解答此题.

 阅读快车系列答案
阅读快车系列答案【题目】甲醇被称为21世纪的新型燃料,工业上通过下列反应①和②,用CH4和H2O为原料来制备甲醇. ①CH4(g)+H2O(g)CO(g)+3H2(g)△H1
②CO(g)+2H2(g)CH3OH(g)△H2
将0.20mol CH4(g)和0.30mol H2O(g)通入容积为10L的密闭容器中,在一定条件下发生反应①,达到平衡时,CH4的转化率与温度、压强的关系如图.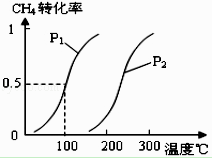
(1)温度不变,缩小体积,增大压强,①的反应速率(填“增大”、“减小”或“不变”),平衡向方向移动.
(2)温度升高,反应①的△H10(填“<”、“=”或“>”),其平衡常数表达式为K= , 100℃时的平衡常数值是 .
(3)在压强为0.1MPa条件下,将a mol CO与 3a mol H2的混合气体在催化剂作用下进行反应②生成甲醇.为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中.请在下表空格中填入剩余的实验条件数据.
实验编号 | T(℃) | n (CO)/n(H2) | P(MPa) |
I | 150 | 1/3 | 0.1 |
II | 5 | ||
III | 350 | 5 |