题目内容
【题目】铜及其化合物在生产、生活中应用广泛。回答下列问题:
(1)用新制Cu(OH)2与葡萄糖反应可制备Cu2O,该反应中葡萄糖是___________(填“氧化剂”或“还原剂”)。
(2)用H2O2、H2SO4混合溶液浸泡废铜屑可制备CuSO4,实现“变废为宝”。若将该反应设计成原电池,则正极的电极反应式为________________。
(3)氧化亚铜(CuCl)是微溶于水、易被氧化的白色固体,广泛用作有机合成催化剂、化学分析试剂等。用NH4NO3氧化海绵铜(含Cu和CuO)制备氯化亚铜的部分流程如下:
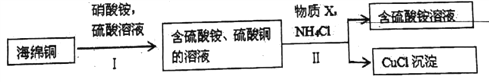
①步骤Ⅰ中,当0.2molNH4NO3参加反应时,反应中有1mol电子发生转移,则铜参加反应的离子方程式为________________________。
②步骤Ⅱ中充分反应后,分离出产品的方法是_________________。
③步骤Ⅱ中物质X可选用_________________(填字母)
a.SO2 b.Cl2 c.H2O2 d.(NH4)2SO3
该物质需过量的原因之一是加快反应速率,另一原因是__________________。
【答案】 还原剂 H2O2+2e-+2H+= 2H2O 5Cu+2NO3-+12H+=5Cu2++N2↑+6H2O 过滤 d 防止CuCl被氧化(合理即给分)
【解析】(1)考查醛基的性质,葡萄糖中含有醛基,被新制氢氧化铜悬浊液氧化,葡萄糖为还原剂;(2)考查电极反应式的书写,发生的反应是Cu+H2O2+H2SO4=CuSO4+2H2O,根据原电池的工作原理,正极上发生还原反应,即电极反应式为H2O2+2H++2e-=2H2O;(3)考查化学工艺流程,①0.2molNH4NO3参加反应时,反应中有1mol电子发生转移,NO3-中N的化合价变化了1/0.2=5,即NO3-中N被还原成0价,转化成N2,离子反应方程式为5Cu+2NO3-+12H+=5Cu2++N2↑+6H2O;②步骤II得到溶液和沉淀,此操作步骤为过滤;③CuSO4→CuCl,Cu的化合价降低,因此所加物质X为还原剂,a、通入SO2,发生2Cu2++SO2+2H2O+2Cl-=2CuCl↓+SO42-+4H+,最后生成硫酸,不符合流程,故a错误;b、Cl2具有强氧化性,故b错误;c、H2O2主要体现氧化性,故c错误;d、(NH4)2SO3中SO32-具有还原性,能与Cu2+发生氧化还原反应,生成CuCl,故d正确;CuCl易被氧化,因此(NH4)2SO3的目的一是加快反应速率,二是防止CuCl被氧化。

 名校课堂系列答案
名校课堂系列答案【题目】人们常用催化剂来选择反应进行的方向.如图所示为一定条件下1mol CH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去].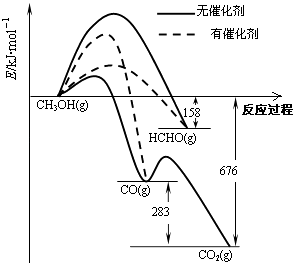
(1)①在有催化剂作用下,CH3OH与O2反应主要生成(填“CO、CO2”或“HCHO”).2HCHO(g)+O2(g)═2CO(g)+2H2O(g)△H= .
②甲醇制取甲醛可用Ag作催化剂,含有AgCl会影响Ag催化剂的活性.用氨水可以溶解除去其中的AgCl,写出该反应的离子方程式: .
(2)已知:CO(g)+2H2(g)CH3OH(g)△H=﹣a kJmol﹣1 .
①经测定不同温度下该反应的平衡常数如下:
温度(℃) | 250 | 300 | 350 |
K | 2.041 | 0.270 | 0.012 |
若某时刻、250℃测得该反应的反应物与生成物的浓度为c(CO)=0.4molL﹣1、c(H2)=0.4molL﹣1、c(CH3OH)=0.8molL﹣1 , 则此时v正v逆(填“>”、“<”或“=”).
②某温度下,在体积固定的2L的密闭容器中将1mol CO和2mol H2混合,测得不同时刻的反应前后压强关系如下:
时间(min) | 5 | 10 | 15 | 20 | 25 | 30 |
压强比(P后/P前) | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
则0~15min,用H2表示的平均反应速率为 , 达到平衡时CO的转化率为 .
(3)利用钠碱循环法可除去SO2 , 消除SO2对环境的污染.吸收液吸收SO2的过程中,pH随n(SO32﹣):n(HSO3﹣)变化关系如下表:
n(SO32﹣):n(HSO3﹣) | 91:9 | 1:1 | 1:91 |
pH | 8.2 | 7.2 | 6.2 |
①根据上表判断NaHSO3溶液显性.
②在NaHSO3溶液中离子浓度关系正确的是 (填字母).
a.c(Na+)=2c(SO32﹣)+c(HSO3﹣)
b.c(Na+)>c(HSO3﹣)>c(H+)>c(SO32﹣)>c(OH﹣)
c.c(H2SO3)+c(H+)=c(SO32﹣)+(OH﹣)
d.c(Na+)+c(H+)=c(SO32﹣)+c(HSO3﹣)+c(OH﹣)