题目内容
【题目】将不同量的CO(g)和H2O(g)分别通入体积为2 L的恒容密闭容器中,进行反应:CO(g) + H2O(g) ![]() CO2(g) + H2(g),得到如下三组数据:
CO2(g) + H2(g),得到如下三组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
CO | H2O | CO2 | |||
1 | 650 | 4 | 2 | 1.6 | 5 |
2 | 900 | 2 | 1 | 0.4 | 3 |
3 | 2 | 1 | 0.4 | 1 | |
下列说法不正确的是
A. 该反应的正反应为放热反应
B. 实验1中,前5min用CO表示的速率为0.16 mol/(L·min)
C. 实验2中,平衡常数K=1/6
D. 实验3跟实验2相比,改变的条件可能是温度
【答案】D
【解析】A. 由表中数据可知,实验1中CO的转化率为40%,而实验2中CO的转化率为20%,压强不能使该化学平衡发生移动,由于温度升高使得CO的转化率减小,所以该反应的正反应为放热反应,A正确;B. 实验1中,前5min用CO表示的速率为![]() 0.16 mol/(L·min),B正确;C. 实验2中,平衡混合物中各组分CO、H2O、CO2、H2的浓度分别为0.8mol/L、0.3 mol/L、0.2 mol/L、0.2 mol/L,所以平衡常数K=
0.16 mol/(L·min),B正确;C. 实验2中,平衡混合物中各组分CO、H2O、CO2、H2的浓度分别为0.8mol/L、0.3 mol/L、0.2 mol/L、0.2 mol/L,所以平衡常数K=![]() 1/6,C正确;D. 实验3跟实验2相比,各组分的平衡量没有改变,所以改变的条件不可能是温度,可能是加入了合适的催化剂,D不正确。本题选D。
1/6,C正确;D. 实验3跟实验2相比,各组分的平衡量没有改变,所以改变的条件不可能是温度,可能是加入了合适的催化剂,D不正确。本题选D。

 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案【题目】温度为T1时,在三个容积均为1L的恒容密闭容器中仅发生反应:2NO2(g) =2NO(g)+O2(g) (正反应吸热)。实验测得:v正= v(NO2)消耗= k正c2(NO2) v逆=v(NO)消耗=2v(O2)消耗=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。下列说法不正确的是
容器 编号 | 物质的平衡浓度(mol/L) | 物质的起始浓度(mol/L) | ||
c(NO2) | c(NO) | c(O2) | c(O2) | |
Ⅰ | 0.6 | 0 | 0 | 0.2 |
Ⅱ | 0.3 | 0.5 | 0.2 | |
Ⅲ | 0 | 0.5 | 0.35 | |
A. 温度为T1,反应达平衡时,容器Ⅲ中的平衡常数K=0.8
B. 达平衡时,速率常数和化学平衡常数的关系K= k正/k逆
C. 当温度改变为T2时,若k正=k逆则T21
D. 容器Ⅱ反应达平衡前,v正>v逆
【题目】化学是一门实验科学,化学反应过程中的能量变化和速率变化是中学化学研究的重要内容
Ⅰ.利用如图所示装置测定中和热
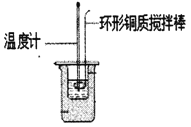
(1)图中明显有一处错误,请指出___________
(2)________(填“能”或“不能”)用Ba(OH)2 溶液和硫酸代替氢氧化钠溶液和盐酸进行中和热测定
Ⅱ.探究硫酸铜的量对氢气生成速率的影响。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积气体所需的时间。
实验 混合溶液 | A | B | C | D | E | F |
4mol/L H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
(1) 请完成此实验设计,其中: V8=_________
(2) 当CuSO4溶液少量时,反应速率明显加快,原因_______
(3) 当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:______________