题目内容
9.Ⅰ、(1)某化学兴趣小组欲从下列装置中选取必要的装置制取(NH4)2SO4溶液,连接的顺序(用接口序号字母表示)是:adef.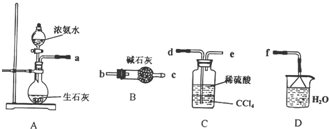
(2)将装置C中两种液体分离开的操作名称是分液.装置D的作用是吸收多余的氨气,防止污染空气,防止倒吸.
Ⅱ、为提高氯化铵的经济价值,我国化学家设计了利用氢氧化镁热分解氯化铵制氨气并得到碱式氯化镁(MgOHCl)的工艺.某同学根据该原理设计的实验装置如图:
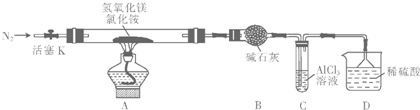
请回答下列问题:
(1)装置A中发生反应生成碱式氯化镁的化学方程式为Mg(OH)2+NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$MgOHCl+NH3↑+H2O,装置B中碱石灰的作用是干燥氨气.
(2)反应过程中持续通入N2的作用有两点:一是使反应产生的氨气完全导出并被稀硫酸充分吸收,二是防止装置C中的AlCl3溶液倒吸入装置B.
(3)装置C的试管中反应的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
分析 Ⅰ.(1)制取的氨气与硫酸反应生成硫酸铵,剩余的氨气用水吸收;
(2)根据分离互不相溶液体操作分析;
从环保和防止倒吸的角度分析;
Ⅱ.(1)根据题意:利用氢氧化镁热分解氯化铵制氨气并得到碱式氯化镁(MgOHCl);碱石灰可以用来干燥氨气;
(2)由于氨气是极易溶于水的,从防倒吸的角度分析;
(3)氨水和氯化铝反应生成氯化铵和氢氧化铝.
解答 解:Ⅰ(1)制取的氨气与硫酸反应生成硫酸铵,剩余的氨气用水吸收,故连接顺序为:a→d→e→f,故答案为:def;
(2)分离互不相溶的液体的方法是:分液;
氨气有刺激性气味,污染空气,用水吸收多余的氨气防止污染空气,加倒置的漏斗防止倒吸,
故答案为:分液;吸收多余的NH3防止污染空气,防止倒吸;
Ⅱ(1)根据题意:利用氢氧化镁热分解氯化铵制氨气并得到碱式氯化镁(MgOHCl),发生的反应为:Mg(OH)2+NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$MgOHCl+NH3↑+H2O,碱石灰可以用来干燥氨气,故答案为:Mg(OH)2+NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$MgOHCl+NH3↑+H2O;干燥氨气;
(2)由于氨气是极易溶于水的,反应过程中持续通入N2,可以使反应产生的氨气完全导出并被稀硫酸充分吸收,并还能防止装置C中的氯化铝溶液倒吸入装置B,
故答案为:防止装置C中的AlCl3溶液倒吸入装置B;
(3)氨水和氯化铝反应生成氯化铵和氢氧化铝,反应的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故答案为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
点评 本题考查了物质的制备方案设计,侧重于学的分析能力和实验能力的考查,注意把握物质转化关系的、物质性质的应用和判断,题目难度中等.

| A. | HOCH2CH2COOH | B. | CH3COOH | C. | HOOC-COOH | D. | 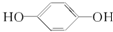 |
| A. | 选择不同催化剂,可以改变反应速率,不改变△H | |
| B. | 及时分离液态硫,能提高SO2的转化率 | |
| C. | 在恒容恒温容器中反应,气体压强不变时达到平衡状态 | |
| D. | 升高温度,正、逆反应速率均增大,n(CO)增大 |
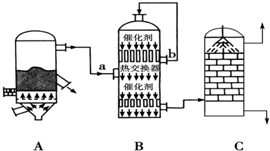
(1)图中设备A的名称是沸腾炉,B设备气流a、b温度较高的是b(填“a”或“b”),C设备中用浓硫酸吸收SO3.
(2)CuFeS2是黄铁矿的另一部分,煅烧时,CuFeS2转化为CuO、Fe2O3和SO2,该反应的化学方程式为:4CuFeS2+13O2$\frac{\underline{\;\;△\;\;}}{\;}$4CuO+2Fe2O3+8SO2.
Ⅱ为了回收利用SO2,研究人员研制了利用低品位软锰矿浆(主要成分是MnO2)吸收高温焙烧含硫废渣产生的SO2废气,制备硫酸锰晶体的生产流程,其流程示意图如下:
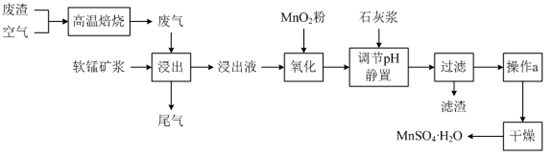
已知,浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子.有关金属离子形成氢氧化物沉淀时的pH见下表:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
| Mn2+ | 8.3 | 9.8 |
(1)写出浸出过程中主要反应的化学方程式:SO2+MnO2=MnSO4.
(2)写出氧化过程中主要反应的离子方程式:2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O.
(3)在氧化后的液体中加入石灰浆,并用pH试纸测定调节pH,pH应调节范围是4.7≤pH<8.3.
(4)滤渣的主要成分有氢氧化铁、氢氧化铝、硫酸钙.
(5)下列各组试剂中,能准确测定尾气中SO2含量的是b、c.(填编号)
a.NaOH溶液、酚酞试液b.稀H2SO4酸化的KMnO4溶液
c.碘水、淀粉溶液d.氨水、酚酞试液.
(1)提出问题:Fe3+、Br2哪一个的氧化性更强?
(2)猜想
①甲同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含Br2(填化学式,下同)所致.
②乙同学认为氧化性:Br2>Fe3+,故上述实验现象是发生化学反应所致,则溶液呈黄色是含Fe3+所致.
(3)设计实验并验证
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的.供选用的试剂:
a.酚酞试液 b.CCl4 c.无水酒精 d.KSCN溶液
请你在下列表格中写出丙同学选用的试剂及实验中观察到的现象.(试剂填序号)
| 选用试剂 | 实验现象 | |
| 方案1 | b | 下层(CCl4层)无色 |
| 方案2 | d | 溶液变为血红色 |
①在足量的稀氯化亚铁溶液中加入l~2滴溴水,溶液呈黄色,所发生的离子反应方程式为2Fe2++Br2═2Fe3++2Br-.
②在FeBr2溶液中通入足量 Cl2,所发生的离子反应方程式为4Fe2++2Br-+3Cl2═4Fe3++Br2+6Cl-.
| A. | NaHS在水中的电离方程式为NaHS═Na++H++S2- | |
| B. | NaHS溶液水解的离子方程式为HS-+H2O═H2S↑+OH- | |
| C. | NaHS溶液与FeSO4溶液反应的离子方程式为S2-+Fe2+═FeS↓ | |
| D. | 向NaHS溶液中滴加过量的新制氯水:HS-+Cl2═S↓+H++2Cl- |
①H2(g)+I2(g)?2HI(g)
②2H2(g)+2I2(g)?4HI(g)
下列说法正确的是( )
| A. | 反应速率用HI表示时,v(HI)=0.008 mol•L-1•min-1 | |
| B. | 两个化学方程式的意义相同,但其平衡常数表达式不同,不过计算所得数值相同 | |
| C. | 氢气在两个反应方程式中的转化率不同 | |
| D. | 第二个反应中,增大压强平衡向生成HI的方向移动 |