题目内容
在0.1 mol/L的醋酸钠溶液中加入等体积的下列物质,溶液中离子浓度大小关系正确的是( )
| A.水;c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| B.0.1 mol/L盐酸;c(Na+)=c(Cl-)>c(H+)>c(CH3COO-)>c(OH-) |
| C.0.1 mol/L醋酸;c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D.0.1 mol/L氢氧化钠;c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
B
解析

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
已知:AgI为黄色沉淀,AgCl为白色沉淀。25℃时,AgI饱和溶液中c(Ag+)为1.22×10-8 mol·L-1;AgCI饱和溶液中c(Ag+)为1.30×10-5mol·L-1。若在5 mL含有KC1和KI浓度均为0.01 mol·L-1的混合溶液中,滴加8 mL0.0l mol·L-1的AgNO3溶液,则下列叙述中不正确的是
| A.溶液中所含溶质的离子浓度大小关系为c(K+)>c(NO3-)>c(Cl-)>c(I-)>c(Ag+) |
| B.溶液中先产生的是AgI沉淀 |
| C.AgCl的KSP的数值为1.69×10-10 |
| D.若在AgI悬浊液中滴加一定量的KCl溶液,黄色沉淀也会转变成白色沉淀 |
在0.1 mol·L-1CH3COOH溶液中存在如下电离平衡:CH3COOH CH3COO-+H+,对于该平衡下列叙述正确的是( )
CH3COO-+H+,对于该平衡下列叙述正确的是( )
| A.加入水时,平衡逆向移动 |
| B.加入少量NaOH固体,平衡正向移动 |
| C.加入少量0.1 mol·L-1盐酸,溶液中c(H+)减小 |
| D.加入少量CH3COONa固体,平衡正向移动 |
已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.0×10-16。下列关于难溶物之间转化的说法中错误的是( )
| A.AgCl不溶于水,不能转化为AgI |
| B.两种难溶物的Ksp相差越大,难溶物就越容易转化为更难溶的物质 |
| C.AgI比AgCl更难溶于水,所以AgCl可以转化为AgI |
D.常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低于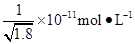 |
将氨水滴加到盛有AgCl浊液的试管中,AgCl逐渐溶解,再加入NaBr溶液又产生了浅黄色沉淀。对上述过程,下列理解或解释中正确的是( )
| A.Ksp(AgCl)<Ksp(AgBr) |
| B.若在AgCl浊液中直接加入NaBr溶液,也会产生浅黄色沉淀 |
| C.上述实验说明AgCl没有NaBr稳定 |
| D.因为Ksp(AgCl)>Ksp(AgOH),故氨水能使AgCl溶解 |
下列说法正确的是( )
| A.25 ℃时NH4Cl溶液的Kw大于100 ℃时NaCl溶液的Kw |
| B.SO2通入碘水中,反应的离子方程式为SO2+I2+2H2O====SO32―+2I―+4H+ |
| C.加入铝粉能产生H2的溶液中,可能存在大量的Na+、Ba2+、AlO2―、NO3- |
| D.100 ℃时,将pH=2的盐酸与pH=12的NaOH溶液等体积混合,溶液显中性 |
已知25 ℃时有关弱酸的电离平衡常数如下表:
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25 ℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
则下列有关说法正确的是( )
A.a mol/L HCN溶液与b mol/L NaOH溶液等体积混合,所得溶液中c(Na+)>c(CN-),则a一定小于b
B.冰醋酸中逐滴加水,则溶液的导电性、醋酸的电离程度、pH均先增大后减小
C.各溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa)
D.在0.1 mol/L CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+)