题目内容
下列有关说法正确的是( )
| A、△H>0的反应一定不能自发进行 | B、同温、同浓度的盐酸和氢氧化钠稀溶液中,水的电离程度相同 | C、牺牲阳极的阴极保护法和外加电流的阴极保护法都是应用电解池原理 | D、恒容密闭容器中进行的反应3A(g)?B(g)+C(g),在其他条件不变情况下,再充入一定量的A气体,A的转化率将减少 |
分析:A、反应自发进行的判断依据是△H-T△S<0;
B、依据溶液中离子积常数分析判断;
C、牺牲阳极的阴极保护法是原电池原理;
D、在其他条件不变情况下,再充入一定量的A气体相当于增大压强,压强增大平衡正向进行;
B、依据溶液中离子积常数分析判断;
C、牺牲阳极的阴极保护法是原电池原理;
D、在其他条件不变情况下,再充入一定量的A气体相当于增大压强,压强增大平衡正向进行;
解答:解:A、△H>0的反应不一定不能自发进行,△H>0,△S>0,高温下△H-T△S<0;故A错误;
B、同温、同浓度的盐酸和氢氧化钠稀溶液中,氢离子和氢氧根离子浓度相同,对水的电离抑制程度相同,水的电离程度相同,故B正确;
C、牺牲阳极的阴极保护法是原电池原理,外加电流的阴极保护法是应用电解池原理,故C错误;
D、恒容密闭容器中进行的反应3A(g)?B(g)+C(g),在其他条件不变情况下,再充入一定量的A气体,相当于增大压强,压强增大平衡正向进行,A的转化率将增大,故D错误;
故选B.
B、同温、同浓度的盐酸和氢氧化钠稀溶液中,氢离子和氢氧根离子浓度相同,对水的电离抑制程度相同,水的电离程度相同,故B正确;
C、牺牲阳极的阴极保护法是原电池原理,外加电流的阴极保护法是应用电解池原理,故C错误;
D、恒容密闭容器中进行的反应3A(g)?B(g)+C(g),在其他条件不变情况下,再充入一定量的A气体,相当于增大压强,压强增大平衡正向进行,A的转化率将增大,故D错误;
故选B.
点评:本题考查了反应自发进行的判断依据,水的电离影响因素分析,金属保护原理的分析应用,平衡移动原理分析,题目难度中等.

练习册系列答案
相关题目
 (2012?绵阳模拟)钾在氧气中燃烧时得到一种钾的氧化物晶体,其结构如图所示,下列有关说法正确的是( )
(2012?绵阳模拟)钾在氧气中燃烧时得到一种钾的氧化物晶体,其结构如图所示,下列有关说法正确的是( )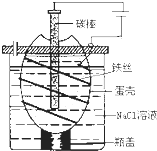 工业上通过电解饱和氯化钠溶液的方法获得氢氧化钠和氯气,图为某实验小组自制的电解饱和食盐水的简易装置,
工业上通过电解饱和氯化钠溶液的方法获得氢氧化钠和氯气,图为某实验小组自制的电解饱和食盐水的简易装置,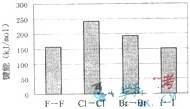 (2009?上海)海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等.
(2009?上海)海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等.