题目内容
【题目】短周期元素X,Y,Z,W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法正确的是( ) 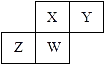
A.原子半径:W>Z>Y>X
B.最高价氧化物对应水化物的酸性:Z>W>X
C.最简单气态氢化物的热稳定性:Y>X>W>Z
D.元素Y,Z形成的化合物是制造光电池的主要材料
【答案】C
【解析】解:短周期元素W的质子数是其最外层电子数的三倍,则W是P元素,根据元素在周期表中的位置关系可确定:X是N元素,Y是O元素,Z是Si元素,
A.同周期原子序数越大原子半径越小,电子层数越多原子半径就越大,所以原子半径大小关系是:Z>W>X>Y,故A错误;
B.元素的非金属性越强,其最高价氧化物对应的水化物的酸性越强,元素的非金属性:X>W>Z,则最高价氧化物对应水化物的酸性:X>W>Z,故B错误;
C.元素的非金属性越强,其相应的氢化物的稳定性就越强,元素的非金属性:Y>X>W>Z,所以元素的氢化物的稳定性:Y>X>W>Z,故C正确;
D.制造光电池的主要材料为Si,而Y、Z形成的化合物为光导纤维的材料,故D错误;
故选C.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目