题目内容
5.能在无色的酸性溶液中大量共存的是下列各组中的离子,( )| A. | Mg2+、SO42-、K+ | B. | ClO -、Na+、Cl- | C. | Cu2+、NO3-、NH4 + | D. | Ag+、NO3-、I- |
分析 酸性溶液中含大量的氢离子,根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应,则离子大量共存,并结合离子的颜色来解答.
解答 解:A.酸性溶液中该组离子之间不反应,可大量共存,故A正确;
B.ClO -、H+、Cl-发生氧化还原反应,不能大量共存,故B错误;
C.Cu2+为蓝色,与无色不符,故C错误;
D.Ag+、I-结合生成沉淀,不能共存,故D错误;
故选A.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
19.下列各组顺序的排列不正确的是( )
| A. | 酸性强弱:H4SiO4>H3PO4>H2SO4 | B. | 还原性:Na>Mg>Al | ||
| C. | 热稳定性:SiH4<PH3<H2S<HCl | D. | 熔点:SiO2>NaCl>I2>CO2 |
20.在中学化学实验中,对某些化学试剂进行循环使用,可以节省资源、减少污染、降低成本.下列做法不合理的是 ( )
| 选项 | 实验名称 | 回收试剂 | 回收方法 | 回收后用途 |
| A | 加热KClO3与MnO2制氧气 | 二氧化锰 | 溶解、过滤、洗涤、干燥 | 重复使用 |
| B | 过氧化钠与水反应 | 氯化钠 | 加入过量盐酸、蒸发、结晶 | 制取实验备用 |
| C | 用CCl4萃取溴水中的溴 | 四氯化碳 | 碱液洗涤、分液 | 重复使用 |
| D | 浓硫酸的稀释 | 稀硫酸 | 直接密封保存 | 制氢气、硫酸盐等 |
| A. | A | B. | B | C. | C | D. | D |
13.下列说法或判断正确的是( )
| A. | 二氧化硅是光纤制品及现代光学的基本原料 | |
| B. | 塑化剂是一种化工塑料软化剂,可以大量添加到婴幼儿玩具中 | |
| C. | 二氧化硅不与任何酸反应,可以用石英做材料制造耐酸容器 | |
| D. | 氢氧化铁溶胶、甘油与乙醇的混合液、含PM2.5的大气均具有丁达尔效应 |
20.下列制备和收集气体的实验装置合理的是( )
| A. |  用氯化铵和氢氧化钙制NH 3 | B. | 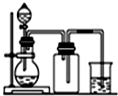 用铜片和稀硝酸制NO | ||
| C. | 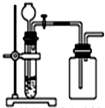 用锌粒和稀硫酸制H 2 | D. | 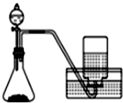 用双氧水和二氧化锰制O2 |
17.如表中关于物质分类的正确组合是( )
| 类别组合 | 酸性氧化物 | 碱性氧化物 | 酸 | 碱 | 盐 |
| A | NO2 | CuO | H2SO4 | NH3•H2O | Na2S |
| B | CO2 | Na2O | CH3COOH | NaOH | NaHCO3 |
| C | SO2 | Al2O3 | HCl | KOH | NaCl |
| D | SO3 | CaO | HNO3 | Na2CO3 | CaCO3 |
| A. | A | B. | B | C. | C | D. | D |
14.下列微粒中,不具有氧化性的是( )
| A. | Cl2 | B. | O | C. | H+ | D. | S2- |
15.用饱和的氯化铁溶液制取氢氧化铁胶体,正确的操作是( )
| A. | 将FeCl3溶液滴入蒸馏水中即可 | |
| B. | 将FeCl3溶液滴入热水中,得到黄色液体即可 | |
| C. | 将FeCl3溶液滴入沸水中,得到红褐色溶液即可 | |
| D. | 将FeCl3溶液滴入沸水中,并继续加热煮沸至生成红褐色沉淀即可 |