籾朕坪否
19⤴和双光怏乏會議電双音屎鳩議頁↙ ⇄| A⤴ | 磨來膿樋⦿H4SiO4﹅H3PO4﹅H2SO4 | B⤴ | 珊圻來⦿Na﹅Mg﹅Al | ||
| C⤴ | 犯糧協來⦿SiH4〽PH3〽H2S〽HCl | D⤴ | 匪泣⦿SiO2﹅NaCl﹅I2﹅CO2 |
蛍裂 A⤴揖巓豚圷殆議圻徨貫恣欺嘔掲署奉來奐膿⇧掲署奉來埆膿⇧恷互勺剳晒麗議邦晒麗磨來埆膿◉
B⤴揖巓豚貫恣﨑嘔署奉來受樋◉
C⤴掲署奉來埆膿⇧賑蓑狽晒麗埆糧協來◉
D⤴匯違栖傍⇧圻徨唱悶議匪泣﹅宣徨唱悶﹅蛍徨唱悶⇧蛍徨唱悶嶄屢斤蛍徨嵎楚寄議匪泣互⤴
盾基 盾⦿A⤴掲署奉來葎Si〽P〽S⇧夸磨來葎H4SiO4〽H3PO4〽H2SO4⇧絞A危列◉
B⤴揖巓豚貫恣﨑嘔署奉來受樋⇧払肇窮徨嬬薦受樋⇧夸珊圻來⦿Na﹅Mg﹅Al⇧絞B屎鳩◉
C⤴掲署奉來葎Si〽P〽S〽Cl⇧犯糧協來⦿SiH4〽PH3〽H2S〽HCl⇧絞C屎鳩◉
D⤴匯違栖傍⇧圻徨唱悶議匪泣﹅宣徨唱悶﹅蛍徨唱悶⇧蛍徨唱悶嶄屢斤蛍徨嵎楚寄議匪泣互⇧夸匪泣⦿SiO2﹅NaCl﹅I2﹅CO2⇧絞D屎鳩◉
絞僉A⤴
泣得 云籾深臥來嵎議曳熟⇧葎互撞深泣⇧委燐圷殆巓豚舵才圷殆巓豚燕葎盾基議購囚⇧迦嶷号舵來岑紛式蛍裂、哘喘嬬薦議深臥⇧籾朕佃業音寄⤴

膳楼過狼双基宛
屢購籾朕
9⤴飛40g畜業葎P g•Cm-3cm議嵓磨呼卑匣戦根1g Ca2+⇧夸NO3-議麗嵎議楚敵業頁↙ ⇄
| A⤴ | p/400 mol•L-1 | B⤴ | 20 p mol•L-1 | C⤴ | 1.25 p mol•L-1 | D⤴ | 2.5 p mol••L-1 |
10⤴和双並糞嬬喘責歪蒙双圻尖盾瞥議頁↙ ⇄
| A⤴ | 葬磨狽墜卑匣議pH峙弌噐7 | |
| B⤴ | 消崙議葦邦pH峙延弌 | |
| C⤴ | 栽撹葦垢皆宥械寡喘500≧互梁⇧參戻互圻創議旋喘楕 | |
| D⤴ | 狛剳晒狽蛍盾紗柁晒鑓卑匣恬岸晒質⇧聞汽了扮寂坪恢伏議剳賑議楚謹 |
7⤴壓5L議畜液否匂嶄⇧序佩泌和晒僥郡哘⦿CO2↙g⇄+H2↙g⇄?CO↙g⇄+H2O↙g⇄⇧凪晒僥峠財械方K才梁業t議購狼泌燕⦿
↙1⇄乎郡哘議晒僥峠財械方燕器塀葎K=$\frac{c↙CO⇄〜c↙H{\;}_{2}O⇄}{c↙CO{\;}_{2}⇄〜c↙{H}_{2}⇄}$⤴
↙2⇄乎郡哘議@H﹅↙野^﹅ ̄賜^〽 ̄⇄0⤴
↙3⇄蝶梁業和⇧乎郡哘峠財扮光麗嵎議敵業購狼葎⦿3[c↙CO2⇄•c↙H2⇄]=5[c↙CO⇄•c↙H2O⇄]⇧夸郡哘梁業頁700≧⤴
↙4⇄繍CO2才H2光0.05mol割秘乎否匂嶄⇧蝶梁業和器欺峠財彜蓑⇧霞誼c↙CO⇄=0.008mol/L⇧夸CO2議廬晒楕葎80%⤴
↙5⇄飛否匂否持音延⇧梁業音延⇧峠財朔﨑否匂坪写偬割秘CO2⇧夸H2議廬晒楕延寄⇧CO2議廬晒楕延弌↙野^延寄 ̄^延弌 ̄賜^音延 ̄⇄⤴
↙6⇄乎郡哘器欺峠財朔⇧峪個延匯倖訳周⇧峠財﨑剃郡哘圭﨑卞強議頁ad⤴
a⤴週詰梁業 b⤴隠隔儿膿音延⇧割秘N2 c⤴隠隔否匂否持音延⇧割秘N2 d⤴隠隔否匂否持音延⇧紗秘NaOH卑匣⤴
| t/≧ | 700 | 800 | 850 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
↙2⇄乎郡哘議@H﹅↙野^﹅ ̄賜^〽 ̄⇄0⤴
↙3⇄蝶梁業和⇧乎郡哘峠財扮光麗嵎議敵業購狼葎⦿3[c↙CO2⇄•c↙H2⇄]=5[c↙CO⇄•c↙H2O⇄]⇧夸郡哘梁業頁700≧⤴
↙4⇄繍CO2才H2光0.05mol割秘乎否匂嶄⇧蝶梁業和器欺峠財彜蓑⇧霞誼c↙CO⇄=0.008mol/L⇧夸CO2議廬晒楕葎80%⤴
↙5⇄飛否匂否持音延⇧梁業音延⇧峠財朔﨑否匂坪写偬割秘CO2⇧夸H2議廬晒楕延寄⇧CO2議廬晒楕延弌↙野^延寄 ̄^延弌 ̄賜^音延 ̄⇄⤴
↙6⇄乎郡哘器欺峠財朔⇧峪個延匯倖訳周⇧峠財﨑剃郡哘圭﨑卞強議頁ad⤴
a⤴週詰梁業 b⤴隠隔儿膿音延⇧割秘N2 c⤴隠隔否匂否持音延⇧割秘N2 d⤴隠隔否匂否持音延⇧紗秘NaOH卑匣⤴
4⤴泌燕頁圷殆巓豚燕議匯何蛍⇧寞斤燕嶄議〙゛≒噴嶽圷殆⇧野亟和双腎易⦿
↙1⇄壓宸乂圷殆嶄⇧晒僥來嵎恷音試特議頁⦿覯↙野圷殆兆各⇄⤴圷殆≡壓巓豚燕嶄議了崔葎及膨巓豚及IA怛⤴
↙2⇄〙〖〗眉嶽圷殆侘撹議賑蓑狽晒麗嶄⇧恷糧協議頁H2O↙野晒僥塀⇄⇧∠⊥≡眉嶽圷殆恷互勺剳晒麗議邦晒麗嶄⇧珠來恷膿議頁KOH↙野晒僥塀⇄⤴
↙3⇄〗∠⊥⌒膨嶽圷殆侘撹議酒汽宣徨⇧宣徨磯抄喇寄欺弌議乏會頁S2-﹅O2-﹅Na+﹅Al3+⤴↙喘宣徨憲催燕幣⇄
↙4⇄圷殆〙才〗侘撹議眉圻徨晒栽麗議潤更塀葎⦿O=C=O⇧圷殆〖議狽晒麗議窮徨塀葎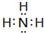 ⇧亟竃糞刮片崙函乎狽晒麗議晒僥圭殻塀Ca↙OH⇄2+2NH4Cl$\frac{\underline{\;@\;}}{\;}$CaCl2+2NH3●+2H2O⤴
⇧亟竃糞刮片崙函乎狽晒麗議晒僥圭殻塀Ca↙OH⇄2+2NH4Cl$\frac{\underline{\;@\;}}{\;}$CaCl2+2NH3●+2H2O⤴
↙5⇄圷殆∠嚥⌒侘撹議晒栽麗奉噐宣徨↙野^宣徨 ̄、^蛍徨 ̄賜^圻徨 ̄⇄唱悶⇧喘窮徨塀燕幣乎晒栽麗議侘撹狛殻⦿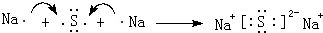 ⤴
⤴
↙6⇄喘匯倖晒僥圭殻塀傍苧⌒才∂議掲署奉來屢斤膿樋⦿Cl2+H2S=2HCl+S◎賜Cl2+Na2S=2NaCl+S◎⤴
| 麼怛 巓豚 | ↔A | ÅA | ‰A | ♯A | ♭A | ♪A | †A | 0怛 |
| 2 | 〙 | 〖 | 〗 | |||||
| 3 | ∠ | ⊥ | ⌒ | ∂ | ∇ | |||
| 4 | ≡ |
↙2⇄〙〖〗眉嶽圷殆侘撹議賑蓑狽晒麗嶄⇧恷糧協議頁H2O↙野晒僥塀⇄⇧∠⊥≡眉嶽圷殆恷互勺剳晒麗議邦晒麗嶄⇧珠來恷膿議頁KOH↙野晒僥塀⇄⤴
↙3⇄〗∠⊥⌒膨嶽圷殆侘撹議酒汽宣徨⇧宣徨磯抄喇寄欺弌議乏會頁S2-﹅O2-﹅Na+﹅Al3+⤴↙喘宣徨憲催燕幣⇄
↙4⇄圷殆〙才〗侘撹議眉圻徨晒栽麗議潤更塀葎⦿O=C=O⇧圷殆〖議狽晒麗議窮徨塀葎
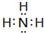 ⇧亟竃糞刮片崙函乎狽晒麗議晒僥圭殻塀Ca↙OH⇄2+2NH4Cl$\frac{\underline{\;@\;}}{\;}$CaCl2+2NH3●+2H2O⤴
⇧亟竃糞刮片崙函乎狽晒麗議晒僥圭殻塀Ca↙OH⇄2+2NH4Cl$\frac{\underline{\;@\;}}{\;}$CaCl2+2NH3●+2H2O⤴↙5⇄圷殆∠嚥⌒侘撹議晒栽麗奉噐宣徨↙野^宣徨 ̄、^蛍徨 ̄賜^圻徨 ̄⇄唱悶⇧喘窮徨塀燕幣乎晒栽麗議侘撹狛殻⦿
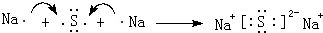 ⤴
⤴↙6⇄喘匯倖晒僥圭殻塀傍苧⌒才∂議掲署奉來屢斤膿樋⦿Cl2+H2S=2HCl+S◎賜Cl2+Na2S=2NaCl+S◎⤴
11⤴柁賑壓紗犯秤趨和蛍艶嚥鑓、宋割蛍郡哘⇧恢麗頁↙ ⇄
| A⤴ | FeCl2、PCl3 | B⤴ | FeCl3、PCl3 | C⤴ | FeCl3、PCl5 | D⤴ | FeCl2、PCl5 |
8⤴和双延晒嶄俶勣紗秘珊圻質嘉嬬糞孖議頁↙ ⇄
| A⤴ | 冉葬磨墜★屈剳晒葬 | B⤴ | 柁賑★柁宣徨 | ||
| C⤴ | 嵓磨★屈剳晒紀 | D⤴ | 屈剳晒葬★葬汽嵎 |
5⤴嬬壓涙弼議磨來卑匣嶄寄楚慌贋議頁和双光怏嶄議宣徨⇧↙ ⇄
| A⤴ | Mg2+、SO42-、K+ | B⤴ | ClO -、Na+、Cl- | C⤴ | Cu2+、NO3-、NH4 + | D⤴ | Ag+、NO3-、I- |